
O agente causal do mofo branco (Sclerotinia sclerotiurum) é considerado um dos patógenos mais importantes no mundo e está distribuído em todas as regiões produtoras, sejam temperadas, subtropicais ou tropicais. Nas safras 2004/05 e 2005/06, as condições para mofo branco no sudoeste Goiano foram ideais observando-se muitos campos de soja afetados e com perdas de rendimento de grão até 20%. Os incrementos da incidência e severidade do fungo Sclerotinia sclerotiurum são motivo de preocupação por produzir corpos reprodutivos de resistência (escleródios) que podem contaminar facilmente áreas não infectadas, porque as estruturas sobrevivem no solo por muitos anos e não se possui material genético resistente a esta doença. A fase mais vulnerável vai do estádio da floração plena (R2) ao inicio da formação das vagens (R3/R4). O fungo é capaz de infectar qualquer parte da planta, porem, as infecções iniciam-se com mais freqüência a partir das inflorescências e das axilas das folhas e ramos laterais (KIMATI, H. et al, 2005).
Ate o momento são descritos 456 patógenos fúngicos que atacam a cultura da soja no mundo (Farr e Rosman, 2010), levando em consideração a importância econômica da cultura, torna-se necessário um controle eficiente desses patógenos, visando aumentar a produção das lavouras de grãos.
O objetivo deste trabalho é identificar e descrever a ocorrência do mofo branco na cultura da soja levando em consideração aspectos da sintomatologia, etiologia, epidemiologia e controle.
Na fazenda Paraíso município de Vianópolis, GO foi coletado material infectado com o patógeno presente nas hastes da soja, em março de 2010. Em seguida o material foi levado para laboratório de Microbiologia do Instituto Federal Goiano – campus Urutaí para análise, identificando o patógeno e colocando o material em câmara úmida.
No Laboratório de Microbiologia do IF Goiano campus Urutaí, foi analisada hastes da soja, com auxilio do microscópio estereoscópio (lupa), as quais apresentavam sinais da doença mofo branco, no qual foi colocado em câmera úmida para crescimento do fungo, após o período de crescimento este foi retirado através do método de pescagem direta para confeccionar duas placas de Petri, contendo meio de cultura BDA para desenvolvimento micelial, após o crescimento e desenvolvimento em placas foi observado a presença de estruturas fúngicas e estas fotografadas.
Os sintomas da planta foram fotografados, primeiramente utilizando microscópio estereoscópio (lupa) e os sinais foram fotografados utilizando câmera digital CiberShot.
Hospedeiro/cultura:Soja (Glycine max L.)
Família Botânica: Papilionoideae
Doença: Mofo branco
Agente Causal (Teleomorfo): Sclerotinia sclerotiorum (Lib.) de Bary
Local de Coleta: Fazenda Paraíso, Vianópolis, GO.
Data de Coleta: 02/03/10
Taxonomia: Pertence ao reino fugi filo Ascomycota, classe Discomycetes, ordem Helotiales, família Sclerotiniaceae, gênero Sclerotinia. Anamorfo: Fungos mitospóricos, grupo dos hifomicetos.
Sintomatologia:
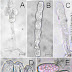
Lesões encharcadas nas folhas, hastes, flores e frutos, o micélio é cotonoso, escleródio (agregado de hifas) é circular, caracteriza-se por ser a estrutura de sobrevivência do fungo.
O fungo ataca toda a parte aérea da planta, principalmente no início da floração ou após a polinização das flores. O primeiro indício da presença da doença é o aspecto murcho da planta. Nos órgãos infectados são encontradas lesões encharcadas, de coloração parda e consistência mole, com micélio branco de aspecto cotonoso, cobrindo os tecidos da planta. Com o progresso da doença, as folhas e caules infectados tornam-se marrons e permanecem eretos mesmo com a morte da planta.
Etiologia (Sinais):
As sinonímias desse patógeno são as seguintes: Hymenoscyphus sclerotiorum (Lib.) W. Phillips, Peziza sclerotiorum Lib., Sclerotinia libertiana Fuckel, Sclerotium varium Pers., Whetzelinia sclerotiorum (Lib.) Korf & Dumont (Índex Fungorum, 2010).
Já foram identificadas várias formas de especialização de patogenicidade dessa espécie. As formas especiais descritas são, Sclerotinia sclerotiorum f. intermedia L.H. Purdy, Sclerotinia sclerotiorum f. major L.H. Purdy, Sclerotinia sclerotiorum f. minor L.H. Purdy, Sclerotinia sclerotiorum f. orobanches Naras. & Thirum. 1954. As variedades especializadas conhecidas são as seguintes, Sclerotinia sclerotiorum var. hyacinthi Fr., Sclerotinia sclerotiorum var. minor L.H. Purdy, Sclerotinia sclerotiorum var. opuntiarum (Speg.) Alippi, Sclerotinia sclerotiorum var. sclerotiorum (Lib.) de Bary 1884 (Index Fungorum, 2010).
No campo os maiores danos da doença são ocasionados pela fase anamórfica e estéril. Esta esterilidade está explicada pela ausência de produção de conídios nesta fase anamórfica predominante nos preríodos monocíclicos da doença. Podem formar estruturas de resistência denominadas de escleródios que quando depositados no solo, sob condições de alta umidade e temperaturas variando de 10-25 °C germinam e desenvolvem, na superfície do solo, os apotécios, que representam o início da fase teleomórfica. Estes produzem as ascósporos que são liberados ao ar e são responsáveis pela infecção das plantas. A transmissão por semente pode acorrer tanto através de micélio dormente (interno) quanto escleródios misturados as sementes. A sobrevivência e a disseminação do fungo são, portanto, realizada através das hifas e dos escleródios (Görgen et al., 2009).
Epidemiologia
No mundo o parasita está distribuído por todos os continenttes, sendo encontrado na África do Sul, Austrália, Brasil, Bulgária, Canadá, China, Grécia, Coréia, México, Nova Zelândia, Nigéria, Portugal, Romênia e Taiwan (Farr e Rosman, 2010).
Apresenta uma forma parasitária, que ocorre na planta hospedeira, e uma fase saprofítica, que incide sobre a matéria orgânica. A fase saprofítica corresponde a sobrevivência do patógeno na ausência de seu hospedeiro. Nessa fase os patógenos sobrevivem em restos de cultura ou em matéria orgânica do solo, na forma de micélio, escleródio. Estes fungos têm a capacidade de persistir no solo durante longos períodos, pois, sob condições normais, crescem na matéria orgânica, e em ambientes favoráveis, mantém-se viáveis através das estruturas de resistência (Görgen et al., 2009).
A partir da fonte de inoculo, representadas por restos de cultura e matéria orgânica, por plantas daninhas, pode ocorrer a disseminação, ativa ou passiva, das estruturas fúngicas. Na disseminação ativa, os zoósporos deslocam-se através da água presente no solo. A forma passiva é realizada através da água (enxurrada ou respingos), do movimento do solo (aração e gradagem) e do tranporte de material infectado (mudas e sementes), promovendo a disseminação dos propágulos a longas distâncias (Nunes Júnior et al., 2007).
O agente causal desta enfermidade (Sclerotinia sclerotiorum) é um patógeno que possue vários hospedeiros, devido a isso a utilização de cultivares resistentes, é uma prática quase impossível, devido a gama de hospedeiros que o patógeno parasita. Tem-se registro de patogenicidade no Brasil de Sclerotinia sclerotiorum nos seguintes hospedeiros; Allium sativum L. (alho), Amaranthus spp., Argemone mexicana L., (papoula do méxico), Arracacia xanthorrhiza Bancr., (batata baroa), Aster ericoides Lam. Bidens pilosa Linn., (picão preto), Borreria alata DC., (erva quente), Brassica alba Boiss. (mostarda-branca), Brassica campestris Hegetschw. (colza), Brassica napus L. var. oleifera Moench (canola), Brassica napus L. (colza), Brassica oleracea Linn. var. botrytis (couve-flor), Brassica oleracea Linn. var. gemmifera, Brassica oleracea Linn. var. itálica (brócolis), Brassica oleracea Linn. (couve), Brassica oleracea var. capitata L. (repolho), Brassica pekinensis Skeels (couve-chinesa), Brassica rapa L. (nabo), Brassica rapa Linn. subsp. rapa, Brassica sp. Tourn. ex L., Capsicum annuum L. (pimentão), Capsicum spp. Tourn. L., Cichorium endivia L. (chicória), Citrus sp. L., Cucumis melo L. (melão), Cucumis sativus L. (pepino), Cucurbitaceae, Cynara scolymus L. (alcachofra), Daucus carota L. (cenoura), Dendranthema morifolium Tzvelev (crisântemo), Euphorbia heterophylla Desf. (leiteira), Galinsoga parviflora Cav. (picão-branco),
Glycine max (L.) Merr. (soja), Gossypium hirsutum L. (algodão), Helianthus annuus Linn. (girassol), Hibiscus subdariffa L., Ipomoea sp. L., Leonotis nepetifolia Schimp. ex Benth. (cordão-de-frade), Lepidium virginicum L. (mastruço), Lupinus angustifolius Aug.DC. (tremoço-azul), Lycopersicon esculentum Mill. (tomateiro), Melinis minutiflora Beauv. (capim-gordura), Musa paradisiaca L. (bananeira), Musa spp., Nicandra physalodes Gaertn., Nicotiana tabacum L., Passiflora spp., Phaseolus lunatus L. (feijão-de-lima), Phaseolus sp. L., Phaseolus spp. L., Phaseolus vulgaris L. (feijão), Pisum sativum L. (ervilha), Raphanus sativus Linn. (rabanete), Sida rhombifolia L. (vassoura), Solanum gilo Raddi (jiló), Solanum melongena L. (berinjela), Solanum tuberosum L. (batata), Spinacia oleracea Linn. (espinafre), Vigna unguiculata L. Walp. (feijão-fradinho) e Zea mays L. (milho) (EMBRAPA, Banco de Dados Brasileiro de Micologia, 2010).
No Brasil o fungo foi identificado 18 vezes na cultura da soja, a primeira evidência do patógeno em soja (Glycine max) foi em 1977. Primeiramente foi denominada como podridão-branca-da-soja, sendo observado também em sementes (EMBRAPA, Banco de Dados Brasileiro de Micologia, 2010), atualmente é conhecida como mofo-branco-da-soja. Em território brasileiro observou-se cientificamente o patógeno associado à cultura da soja nos estados de Minas Gerais, Paraná, Rio Grande do Sul e Distrito Federal (EMBRAPA, Banco de Dados Brasileiro de Micologia, 2010).
Controle
O tratamento de sementes com fungicidas é uma prática utilizada, plantar em áreas com solos de boa drenagem, dar preferência a materiais de crescimento determinado, aumentar espaçamento quando possível, pois melhora a aeração, manejo de Irrigação, qualidade do equipamento de pulverização e irrigação. Rotação de cultura através de sistemas de integração, que utilizam depois do cultivo da soja espécies resistentes como o milho e a braquiária é um método utilizado para diminuir os efeitos maléficos de diversos patógenos (Sistema Santa Fé) (Kluthcouski et al., 2003).
Com o objetivo de integrar a palhada de Braquiaria ruziziensis com o controle biológico (Trichoderma harzianum). Sob palhada de braquiária, verificou-se 100% de parasitismo e morte de 70-100% de escleródios e em solo sem cobertura, houve 16-75% de parasitismo com 0-45% de morte de escleródios (Görgen et al., 2009).
Na utilização de produtos fitossanitários (fungicidas), o produto registrado no Ministério da Agricultura Pecuária e Abastecimento (MAPA) e seus respectivos ia. é: Cercobin 500 SC (tiofanato-metílico) (Agrofit, 2010).
Nunes Júnior et al. (2007), em um experimento conduzido em Silvânia - GO, com o objetivo de avaliar a eficácia de fungicidas no controle da doença chegou aos seguintes resultados, quanto à produtividade e à massa de escleródios produzida, os melhores resultados foram observados com dimoxystrobina + boscalid, fluopyram, fluazinam, procimidona e uma formulação de carbendazim a 500 g.ha-1.
Em áreas de ocorrências de mofo branco recomenda-se fazer a rotação/sucessão de soja com espécies resistente como milho, aveia branca ou trigo; eliminar as plantas daninhas que, como já foi mostrado, na maioria, são hospedeiras do fungo; incorporar restos culturais para evitar a fase saprofítica do fungo, fazer adubação adequada; aumentar o espaçamento entre linhas, reduzindo a população ao mínimo recomendado para cada variedade (Alves et al., 2010).
LITERATURA CITADA:
AGROFIT, 2010, Disponível em http://extranet.agricultura.gov.br/agrofit_cons/principal_agrofit_cons. Acessado em junho de 2010.
EMBRAPA/CNPAF; IHARABRAS. S.A. INDS. QUIM.- MIRANDA. E.R.R. H. Kimati, L Amorim, A Bergamim Filho. Manual de fitopatologia volume 1 , Ceres
EMBRAPA Banco de Dados Brasileiro de Micologia. Disponível em:
INDEX FUNGORUM. Disponível em:
KIMATI, H.; AMORIM, L.; REZENDE, J.A.M.; BERGAMIN FILHO, A.; CAMARGO, L.E.A.; Manual de fitopatologia: Doenças das plantas cultivadas 4ª Ed.vol. 2, p. 580– São Paulo: Agronômica Ceres, 2005.
ALVES, R.C., DEL PONTE, E.M. Requeima da batata. In: Del Ponte, E.M. (Ed.) Fitopatologia.net - herbário virtual. Departamento de Fitossanidade. Agronomia, UFRGS. Disponível em: http://www.ufrgs.br/agronomia/fitossan/herbariovirtual/ficha.php?id=101. Acesso em: 02 ago 2010.
KLUTHCOUSKI J., STONE L. F., AIDAR H. Integração lavoura-pecuária– Santo Antônio de Goiás: Embrapa Arroz e Feijão, 2003. 570 p. : il. color..
FARR & ROSMAN, SBML Systematic Botany of Mycological Resources. Disponível em:
GÖRGEN, C.A., LOBO JR., M., GONTIJO, G.H.A., PIMENTA, G., CARNEIRO, L.C. Manejo integrado do mofo branco da soja utilizando Trichoderma harzianum e palhada de Brachiaria ruziziensis. Universidade Federal de Goiás – Campus Jataí. Fitopatologia Brasileira, Maringá, Vol32, p.367, 2007.Suplemento.
NUNES JÚNIOR, J., PIMENTA, C.B., NUNES SOBRINHO, J.B., FERREIRA, L.C., COSTA, N.B., ANDRADE, P.J.M., MEYER, M.C.. Avaliação da eficácia de fungicidas no controle de mofo branco (Sclerotinia sclerotiorum) em soja, no Estado de Goiás. CTPA, SEAGRO-GO. Fitopatologia Brasileira, Maringá, Vol32, p.367, 2007.Suplemento




Nenhum comentário:
Postar um comentário
Observação: somente um membro deste blog pode postar um comentário.