Autor: Marco Antonio de Resende Moraes
O fungo Plasmopara viticola, sinônimo de Botrytis viticola, causador da doença Míldio, afeta, além de muitas espécies de Vitis, plantas como Ampelopsis heterophylla, A. brevipedunculata, Partenocissus quinquefolia e P. tricuspidata (Kimat e Galli, 1980).
São 194 o número de espécies do fungo Plasmopara viticola, 18 variedades e 23 formae especiales registradas na literatura para este gênero (Índex Fungorum, 2010). No Brasil o fungo Plamospara viticola ataca afeta principalmente os estados São Paulo, Rio Grande do Sul, Espírito Santo, Santa Catarina, Paraná, Ceará (Cernagen, 2010).
São 1300 gêneros de Plasmopara, 3 espécies de Plasmopara viticola, que são: Ampelopsis brevipendulata var. heterophylla, Ampelopsis sp, Ampelopsis brevipedunculata (Index fungorum, 2010).
Os sintomas do míldio iniciam-se por um encharcamento do mesofilo, formando o sintoma conhecido por “mancha de óleo”, uma mancha pálida, pequena, de bordos indefinidos, mais facilmente visíveis por transparência contra a luz. Em condições de alta umidade (acima de 95%), na face inferior da folha, sobre a mancha de óleo, observa-se uma eflorescência branca, densa, de aspecto cotonoso, constituídas pela frutificação do fungo Plasmopara viticola. Este sintoma é conhecido por “mancha branca” ou “mancha mofo”.
O fungo pertence à classe dos Ficomicetos. É parasita obrigatório e nos tecidos dos hospedeiros produz, através dos estômatos, esporangióforos ramificados, monopodialmente, que suportam esporângios ovalados característicos (Kimati e Galli, 1980).
Com o passar do tempo, a área infectada necrosa e as manchas tornam-se avermelhadas. As lesões necróticas são irregulares e podem coalescer, ocupando grande área do limbo foliar. Folhas severamente infectadas geralmente caem. Esta desfolha reduz o acumulo de açúcar nos frutos e enfraquecem a planta, comprometendo a produção do ano seguinte (Amorim e Kuniyuki, 2005).
Nas inflorescências infectadas ocorre o escurecimento da ráquis, podendo ainda haver esporulação do fungo, seguido pelo secamento e queda dos botões florais. Quando o fungo ataca as bagas mais desenvolvidas, estas são infectadas pelos pedicelos e o fungo se desenvolve no interior da baga, tornando-as escuras, duras, com superfícies deprimidas, provocando a queda das mesmas. Este sintoma nesta fase de desenvolvimento é denominado de "míldio larvado" ou "grão preto" (Sônego,1980).
Nos tecidos do hospedeiro, P. viticola cresce intercelularmente através de hifas cenocíticas (8-10 µm de diâmetro) emitindo haustórios globosos ao interior das celular parasitadas. Em frutos jovens, os esporangioforos emergem pelas lenticelas. A formação destas estruturas requer 95-100% de umidade relativa, pelo menos quatro horas de escuro, e ocorre preferencialmente no intervalo de temperatura de 18-22 ºC. Os esporangioforos destacam-se com facilidade dos esporangioforos e são disseminados pelo vento ou respingos de chuva. Cada esporângio da origem a 1 a 10 zoósporos (6-8 x 4-5 um) biflagelados. Esta estrutura na presença de água movimenta-se na superfície do hospedeiro e encistam próximo ao estômato. Logo após encistar, o fungo P. viticola emite um tubo germinativo que penetra no hospedeiro. Zoospóros são preferencialmente unicelulares e fusões protoplasmáticas de hifas oriundas de diferentes zoósporos podem ocorrer dentro dos tecidos parasitados, dando origem a micélio heterocariotico (Amorim e Kuniyuki, 2005).
O agente causal do míldio da videira pertence ao reino: Chromista, divisão: Oomycota, classe: Oomycetes, sub. Classe: Peronosporomycetidae, ordem: Peronosporales, família: Peronosporaceae.
Classe Oomycetes: esse grupo peculiar de fungos, salvo raras exceções, não apresenta quitina na sua parede celular e, sim, celulose. Glucanas são os principais componentes da sua parede celular. Os oomycetes são caracterizados através da sua reprodução assexual, pela formação de zoósporos biflagelados, tendo um flagelo do tipo chicote e outro do tipo tinsel. Os oósporos são formados dentro ou a partir de esporângios, que variam de forma conforme os gêneros e espécies de fungos envolvidos. O talo dos oomycetes é micelial, bem desenvolvido, diplóide, com hifas asseptadas, a reprodução sexual é caracterizada pela formação de oósporos, esporo de repouso diplóide, de parede espessa, originário de fecundação do oogônio (gametângio feminino) pelo anterídio (gametângio masculino) (Krugner e Bacchi, 1995). Família Peronosporaceae: contém um total de 7 gêneros abrangendo cerca de 600 espécies. Esta família inclui espécies que produzem bolor e mofo azul. A família contém patógenos de plantas necessário. Parasitismo é realizado através da utilização de haustórios, que são estruturas especializadas que são capazes de penetrar nos tecidos do hospedeiro. Em geral, as plantas parasitas são dicotiledôneas. O Peronosporaceae ter alguma importância econômica, uma vez que incluem espécies que têm sexo micorrízicos plantas parasitas utilizados em culturas agrícolas. Alguns exemplos destes tipos de protistas são: Plasmopara viticola , Peronospora tabacina e Bremia lactucae que produzem doenças em uvas , rapé e alface, respectivamente (Alexopolous et al.2010).
A reprodução assexual ocorre através dos estômatos, com a emissão de esporangióforos (140-250 µm de comprimento), ramificados monopodialmente, que produzem esporângio ( 14 x 11 µm), ovalados e hialinos. Cada esporângio da origem a 1 a 10 zoósporos (6-8 x 4-5 µm), biflagelados. A fase sexuada do agente causal ocorre dentro dos tecidos do hospedeiro, principalmente nas folhas. Com a decomposição dos tecidos do hospedeiro, os oósporos são liberados durante o inverno. A disseminação ocorre por ocorre por respingos de chuva e pelo vento. A fase sexuada é a principal forma de sobrevivência do fungo nos países temperados, embora no Brasil, a sobrevivência possa se dar por micélio no interior dos tecidos vivos. O fungo pode completar seu ciclo em apenas 4 dias (Amorim e Kuniyuki, 2005).
O objetivo deste trabalho é apresentar aspectos gerais e morfológicos do fungo Plasmopara viticola.
O trabalho foi realizado no Laboratório de Microbiologia do IFGoiano campus Urutaí, GO.
O fungo foi retirado da folha de uva coletada na região de Ipameri e Urutaí – GO,. Analisou-se sintomas nas respectivas folhas, foi preparado lâminas semi-permanentes pelo método de pescagem utilizando microscópio estereoscópio, usando azul algodão como corante (composição : ácido acético, ácido lático, glicerina e água destilada, composição do corante: água destilada e etanol), Na lâmina com adição fixador lactofenol cooton-blue (62,5 mL ácido lático, 2,6 mL ácido acético, 100 mL água e 100 mL glicerina), depositou-se fragmentos de estruturas fúngicas para conservação das estruturas do fungo, em seguida coberta com lamínula e vedada com esmalte.
Essa lâmina foi levada ao microscópio ótico para visualização das estruturas fúngicas, observado como características a formação de esporangióforos e esporângios nas extremidades, sendo considerado um falso fungo, microfotografado foram tiradas no microscópio estereoscópico e ótico. Os registros micro e macrofotográficos foram realizados utilizando câmera digital Canon® modelo Power Shot A580.

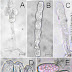
Figura 1: Míldio de videira(plasmopara viticula) incidente em uva(Vitis vinícola) A. esporangio: (bar = 1 µm), B: esporangióforo: (bar = 28 µm), C: esporângio ligado ao esporangioforo, D: esporângio, esporangioforo: (bar = 4 µm), E: trios, F: frutificação de Plasmopara viticola na parte inferior da folha, G: mancha de "óleo" de míldio
Descrição Micológica
O fungo Plasmospora viticola possui ascas em lóculos. Os ascósporo são hialinos, tri-septados, de dimensão aproximada de 15,5 x 1,25 µm. Os lóculos são desprovidos de ostíolo e, portanto, os ascósporos são liberados pela desintegração do estroma. Na sua fase imperfeita forma conídios unicelulares, hialinos, oblongos a ovóides, de 2,5 x 5,5 µm de dimensão, em acérvulos, sobre uma base estromática. Os conídios são produzidos na fase de crescimento vegetativo da videira, sob condições não foi observada a fase perfeita. O fungo sobrevive de um ano para outro nas lesões dos sarmentos e gavinhas, bem como nos restos de cultura no solo, onde, no inicio da estação produz conídios e mais raramente, ascósporos.
LITERATURA CITADA
AMORIM, L. E KUNIYUKI, H. Doenças de videiras In: kimati,H.; Amorim, L.; Rezende, J. A. M.; Bergamin Filho, A.; Camargo, L. E. A.; Manual de Fitopatologia, doenças das plantas cultivadas.Ed. Ceres, São Paulo-SP. 2ª Ed. 2005.
KRUGER, T. L. & BACHI, L. M. A. Fungos In: Bergamin Filho, A.; Kimati, H. ; Amorim,L. , Manual de Fitopatologia. Volume I: Princípios e conceitos. Terceira edição. Editora agronômica Ceres Ltda,1995.São Paulo-SP.
KIMAT, H.; GALLI, F. Doenças de videiras. In: Galli F., Carvalho T.C.P., Tokerhi H., Balmer E., Kimat H., Cardoso N.O.C., Salgado L.C., Krungner L.T., Cardoso N.B.J.E., Bergaminho Filho A., Manual de Fitopatologia, Doenças de plantas cultivadas. Ed. Agronômica Ceres LTDA, Sao Paulo-SP. Volume II. 1980.
Disponível em: http://www.ncbi.nlm.nih.gov/pubmed/18396827 Acessado em:29 de abril de 2010.
INDEX FUNGORUM Disponivel em: http://www.indexfungorum.org/names/names.asp , acessado em 24 de junho de 2010.
CENARGEN disponível em: http://www.cenargen.embrapa.br
Farr, D.F., & Rossman, A.Y. Fungal Databases, Systematic Mycology and Microbiology Laboratory, Disponível em:http://nt.ars-grin.gov/fungaldatabases/ acessado em 29 de junho de 2010.


Revisar informações. Trata-se de um PSEUDOFUNGO, do reino Chromista.
ResponderExcluir