Esta página está sob responsabilidade do professor Dr. Milton Luiz Paz Lima, maiores considerações aponte comentários nas publicações sinta-se a vontade para escrever para milton.lima@ifgoiano.edu.br
quinta-feira, 29 de abril de 2010
Descrição morfológica de Plasmopara viticola
Família Peronosporaceae: contém um total de 7 gêneros abrangendo cerca de 600 espécies. Esta família inclui espécies que produzem bolor e mofo azul. A família contém patógenos de plantas necessário. Parasitismo é realizado através da utilização de haustórios, que são estruturas especializadas que são capazes de penetrar nos tecidos do hospedeiro. Em geral, as plantas parasitas são dicotiledôneas. O Peronosporaceae ter alguma importância econômica, uma vez que incluem espécies que têm sexo micorrízicos plantas parasitas utilizados em culturas agrícolas. Alguns exemplos destes tipos de protistas são: Plasmopara viticola , Peronospora tabacina e Bremia lactucae que produzem doenças em uvas , rapé e alface, respectivamente (Alexopolous CJ, Charles W. Mims, M. Mims, M. Blackwell et. Blackwell).
Esta doença foi observada pela primeira vez na América em 1834. de 1878 o patogênico foi levada para a Europa em Americana ações, para em setembro do mesmo ano, foi registrado pela primeira vez na França. (B. e C. Berl). And De Toni E De Toni.
A doença é causada pelo fungo Elsinoe ampelina (De Bary) Shear, Ascomiceto que, na sua fase imperfeita, corresponde as espécies Sphaceloma ampelinum De Bary. Elsione ampelina forma asca em lóculos imersos em estroma providos de uma asca por lóculo. Os ascósporos são hialinos, tri-septados, de dimensão aproximada de 15,5 x 1,25 micra. Os lóculos são desprovidos de ostíolo e, portanto, os ascósporos são liberados pela desintegração do estroma. Os conídios são produzidos na fase de crescimento vegetativo da videira. O fungo sobrevive de um ano para outro ano nas lesões dos sarmentos e gavinhas, bem como nos restos de cultura nos solos, onde, no inicio da estação produz conídios e mais raramente, ascósporos. (Kimat, L.; Galli, F.)
É uma parasita obrigatória, da classe Oomycetes, família Peronosporaceae. Nos tecidos do hospedeiro, P. viticola cresce intercelularmente através da hifa cenocítica emitindo haustórios globosos ao interior das células parasitadas. A reprodução assexual ocorre através dos estômatos, com a emissão de esporangióforos, ramificados monopodialmente, que produzem esporângio, ovalados e hialinos. Cada esporângio da origem a 1 a 10 zoósporos biflagelados. A fase sexuada do agente causal ocorre dentro dos tecidos do hospedeiro. A fase sexuada é a principal forma de sobrevivência do fungo nos países temperados, embora no Brasil, a sobrevivência possa se dar por micélio no interior dos tecidos vivos. O fungo pode completar seu ciclo em apenas 4 dias (Amorim, L.; Kuniyuki, H.).
O fungo causador da doença afeta, além de muitas espécies de Vitis, plantas como Ampelopsis heterophylla, A. brevipedunculata, Partenocissus quinquefolia e P. tricuspidata. Doença originaria dos Estados Unidos (Kimat, H.; Galli, F.).
O agente causal do míldio é originário da America do Norte e provocou enormes prejuízos na espécie Vitis vinifera (européia) quando introduzindo no continente europeu em 1875 (Amorim, L.; Kuniyuki, H.)
Classe Oomycetes: esse grupo peculiar de fungos, salvo raras exceções, não apresenta quitina na sua parede celular e, sim, celulose. São caracterizados através da sua reprodução assexual, pela formação de zoósporos biflagelados, tendo um flagelo do tipo chicote e outro do tipo tinsel. O talo dos oomycetes é micelial, bem desenvolvido, diplóide, com hifas asseptadas, a reprodução sexual é caracterizada pela formação de oósporos, esporo de repouso diplóide, de parede espessa, originário de fecundação do oogônio (gametângio feminino) pelo anterídio (gametângio masculino) (T. L., Krugner; Lilian, M. A., Bacchi)
Referencias bibliográficas:
Amorim, L.; Kuniyuki, H. Vitis spp. Kimat, H.; Amorim, L.; Rezende, J. A. M.; Bergamin Filho, A.; Camargo, L. E. A.; Fungos In: Manual de Fitopatologia volume II: doença de plantas cultivadas, quarta edição. Editora agronômica Ceres Ltda, 2005. São Paulo-SP.
Kruger, T. L. & Bachi, L. M. A. Fungos In: Bergamin Filho, A.; Kimati, H. ; Amorim,L. , Manual de Fitopatologia. Volume I: Princípios e conceitos. Terceira edição. Editora agronômica Ceres Ltda,1995.São Paulo-SP.
Kimat, H.; Galli, F., Vitis spp. Manual de Fitopatologia volumeII:Doenças de plantas cultivadas Editora agronômica Ceres Ltda.
Disponível em: http://translate.google.com.br/translate?hl=pt-BR&sl=en&u=http://chestofbooks.com/gardening-horticulture/fruit/Manual-of-Fruit-Diseases/Downy-Mildew-Caused-By-Plasmopara-Viticola-B-And-C-Berl.html&ei=heTYS6f9HoK78gbDxPnpBQ&sa=X&oi=translate&ct=result&resnum=16&ved=0CEcQ7gEwDw&prev=/search%3Fq%3Dplasmopara%2Bviticola%26hl%3Dpt-BR , Acessado em:28 de abril de 2010.
Disponível em: http://translate.google.com.br/translate?hl=pt-BR&sl=es&u=http://es.wikipedia.org/wiki/Peronosporaceae&ei=fenYS-yUH4L78AbsnIyvBQ&sa=X&oi=translate&ct=result&resnum=7&ved=0CCMQ7gEwBg&prev=/search%3Fq%3Dfamilia%2BPeronosporaceae%26hl%3Dpt-BR, Acessado em:28 de abril de 2010.
Aspectos Gerais e Morfológicos do Fungo Cercospora kaki sp.
Os sintomas apresentam-se em ambas as fases das folhas,
O fungo sobrevive nas folhas infectadas que permanecem embaixo das árvo
 res.
res.Cercospora kaki sp. apresenta frutificação na superfície foliar; estroma globular, pardo-escuro, com 40 a 76 µm de diametro; fascículos muito densos; conidióforos oliváceos uniformemente coloridos, estreitos no ápice; conídios oliváceos frequentemente curvados, de base obcônia a obconicamente truncada, ápice obtuso a redondo, com 2 a 7 septos e dimensões de 2-3 x 44-88 µm. A sobrevivência do fungo durante o inverno ocorre nas folhas caídas, que servirão de inóculo inicial durante o período vegetativo do caquizeiro (R.B. Bassanezi, L. Amorim & C.C. Malvas,2005).
Autor: Telismar de Sousa Ribeiro
Microbiologia terceiro Periodo
Referências Bibliográficas:
H. Kimati, L. Amorim, J.A.M. Rezende, A. Bergamin Filho, L.E.A. Camargo Manual de fitopatologia volume 2 , Doenças das plantas cultivadas quarta edição Editora Agronômica Ceres Ltda. São Paulo 2005.
http://extranet.agricultura.gov.br/agrifot_cons/!ap_praga_detalhe_cons?p_id_cultura_praga=4126&p_tipo_janela=NEW, disponivél em: Acessado em 29 de abril de 2010.
Aspectos gerais e morfológicos do fungo Rhizopus sp.
A divisão Zigomycetes apresenta aplanósporos (esporangiósporos imóveis) disseminados pelo vento. A reprodução sexual e caracterizada pela formação de zigósporo.
Os dois gêneros fitopatogenicos da ordem Mucorales, Choanephora e Rhizopus são parasitas fracos. O Rhizopus e um sapróbio habitante de solo, ocorrendo também em frutos, alimentos e outros materiais em decomposição.
Causa podridão em frutos e outros órgãos de reserva carnosos da planta, nas fases de pós colheita, durante o armazenamento, transporte e comercialização desses produtos.
Este fungo produz zigósporos através de seu ciclo sexual, os quais estão envolvidos na sua sobrevivência. E através do ciclo sexual que este fungo mantém continuamente na natureza.Os esporangiósporos facilmente disseminados pelo ar podem se depositar na superfície dos frutos ou outros órgãos de reserva onde germinam e penetram através de ferimentos.
O micélio que é haplóide desenvolve se no interior do hospedeiro, secretando enzimas pectinolíticas e celulolíticas, o que acarreta a desintegração dos tecidos e a podridão mole.
Novos esporângios são longos formados externamente a parti de esporangióforos tendo na base rizóides imersos no hospedeiro. A parti dos rizóides, desenvolvem se hifas aéreas, os estolões, que ao tocar o substrato formam novos rizóides e esporangióforos.
A reprodução de novos esporangiósporos completa o ciclo assexual, (BERGAMIM et al.,1995).

REFERERÊNCIAS BIBLIOGRÁFICAS
A. Bergamim Filho.H. Kimati. L.Amorim. Manual de fitopatologia. Volume 1.princípios e conceitos. 3 edição. Editora Agronômica Ceres 1995 .São Paulo SP.
Cladosporiose do maracujá (Cladosporium herbarum) incidente em folhas de maracujá (Passiflora edulis).
A Cladosporiose do maracujazeiro ou também chamada de verrugose, é causada pelo fungo Cladosporium herbarum, ocorrem sobre inúmeras espécies vegetais, especialmente como componente da micoflora de sementes (Ufrgs, 2010).
É uma doença relativamente importante, que surge principalmente em tecidos mais jovens, danificando o desenvolvimento da planta, e assim causando graves prejuízos em todas as zonas produtoras do maracujá no Brasil. Em viveiros pode causar a morte de mudas, enquanto em lavouras ocasiona má aparência dos frutos, que reduz o valor comercial para consumo in natura (Ufrgs, 2010).
O objetivo deste trabalho é identificar, descrever e apontar medidas de controle de C. hebarum incidente em folhas de maracujá.
Folhas de maracujá apresentando sintomas da cladosporiose foram coletadas no campo experimental do IF Goiano e levadas ao Laboratório de Microbiologia. Utilizando-se o método de “pescagem direta”, preparou-se lâminas semipermanentes utilizando corante azul de algodão. Após confecção da lâmina ela foi observada em microscópio ótico onde, foi analisado as estruturas morfológicas para caracterização. As lâminas semi-permanentes após analisadas foram vedadas com esmalte para visualização.
Hospedeiro/cultura: Maracujá (Passiflora edulis (Sims)).
Família Botânica: Passiflorácea.
Doença: Cladosporiose-do-maracujazeiro.
Agente Causal: Cladosporium herbarum (Pers.) Link (1816).
Local de Coleta: Fazenda Palmital, Urutaí, GO.
Data de Coleta: 21/03/10
Taxonomia: A forma anamórfica pertence ao Reino Fungi, grupo incerto dos fungos mitospóricos, sub-grupo hifomicetos (Kirk et al., 2001). A forma teleomórfica pertence ao Reino Fungi, Divisão Ascomycota, Classe Dothideomycetes, Sub-classe Dothideomycetidae, Ordem Capnodiales, Família Davidiellaceae, Gênero Cladosporium e Espécie Cladosporium herbarum (Index Fungorum, 2010).
Sintomatologia
A doença afeta preferencialmente os tecidos novos de folhas, ramos, flores e frutos. Nas folhas os sintomas manifestam-se no início com pequenas manchas, circulares, inicialmente translúcidas, e posteriormente uma área verde pulverulenta começa a se formar no centro em direção a borda, tornando a mancha obscurecida. Depois, os tecidos da lesão sofrem necrose e caem, ocorrendo as perfurações na folha. Nos ramos e ponteiros os sintomas são inicialmente semelhantes às das folhas, que se convertem em cancro de aspecto alongado, deprimido. Essas lesões são semelhantes a barquinhos de papel emborcados e, nestes locais, pela ação do vento, tornam-se fracos e quebradiços. Nos frutos, as lesões são superficiais, não atingindo as partes internas e, portanto, não afetando a qualidade das sementes e do suco, mas há uma redução do seu valor comercial. As lesões iniciam como diminutos pontos marrom-claros, levemente deprimidos. Pelo crescimento do tecido da casca adjacente à margem da lesão, a área afetada é elevada até um pouco acima do nível da superfície, originando verrugas de coloração palha, que podem coalescer, afetando grande parte da superfície do fruto (Ufrgs, 2010).
Etiologia
O patógeno é considerado um saprófita que se transforma em um patógeno de plantas em diferentes condições de estresse. A infecção do fungo forma uma colônia com estruturas com forma profusa, aveludada, na coloração verde-oliva ou marrom-olivácea. Os conidióforos são retos ou flexuosos, geniculados e sempre nodosos, claros a marrom-oliváceos, lisos, altos, com cerca de 250mm de comprimento e 3 a 6mm de largura. Os conídios são razoavelmente grandes, sempre em longas cadeias ramificadas, forma variando de elipsoidal a oblonga, arredondada em duma das extremidades, de coloração clara a marrom-olivácea, uni ou binucleados. a superfície do conídio apresenta pequenas verrugas bem distintas e apresenta 0-3 septos (Pio-Ribeiro, et al., 1997).
Epidemiologia
O fungo Cladosporium herbarum é um patógeno de plantas. Seus hospedeiros incluem Bryum , Buxbaumia , Gyroweissia , Tortula , e Dicranella (Cenargen, 2010). As sinomínias desse gênero são: Acrosporella Riedl & Ershad, (1977), Azosma Corda, (1831),Didymotrichum Bonord., (1851), Graphiopsis Trail, (1889), Heterosporium Klotzsch ex Cooke, (1877), Hormodendrum Bonord. (1851), Mydonosporium Corda, (1833), Myxocladium Corda, (1837), Polyrhizium Giard., (1889), Spadicesporium V.N. Boriss. & Dvoïnos., (1982), Sporocladium Chevall., (1826). As sinominias da espécie são: Byssus herbarum (Pers.) DC., (1815), Dematium herbarum Pers., (1794), Dematium vulgare Pers., (1822), Heterosporium epimyces Cooke & Massee, (1883). Foram descritas cerca de 500 espécies pertencentes ao gênero Cladosporium (Index Fungorum, 2010).
A disseminação do patógeno se dá através de mudas infectadas e pelo vento. A alta umidade é necessária para que ocorra a infecção, e as folhas jovens são muito mais suscetíveis que as adultas. No Brasil, no inicio da primavera, quando a temperatura é mais amena, a doença é mais severa em ramos e folhas. Temperaturas elevadas proporcionam ao patógeno causar lesões em brácteas e cálices de botões florais, sem prejuízos à frutificação, e em frutos que estejam protegidos pela massa vegetativa, devido ao microclima úmido e com temperaturas amenas (Ufrgs, 2010).
O agente causal é um fungo muito ativo em épocas de temperaturas amenas (15 a 22°C). Em estações ou regiões quentes só causa lesões em frutos devido ao micro clima úmido que se forma pelo envolvimento da massa vegetativa. Em ambientes de temperaturas amenas a cladosporiose é muito prejudicial na brotação primaveril, quando pode comprometer os ramos novos, através de lesões cancróticas, bem como perfurações e engruvinhamentos de folhas, com isso atrasam o início da safra. O mais recomendável é que tais brotações ocorram sob cobertura fitossanitária utilizando-se fungicidas à base de cobre (Yamashiro, 1980).
Controle
Os fungicidas dos grupos triazóis têm - se mostrado bastante eficientes para controle da doença, com diferença na eficiência curativa entre princípios ativos dentro de cada grupo. Existe atualmente quatro produtos químicos registrados no Ministério da Agricultura para o controle dessa doença, sendo eles: Constant tebuconazol (triazol), Elite tebuconazol (triazol), Folicur 200 EC tebuconazol (triazol) e o Triade tebuconazol (triazol) (Agrofit, 2010).
Além do controle químico, é importante considerar o manejo da cultura, devendo utilizar mudas isentas de doença, provenientes de plantações sadias, evitar introduzir em áreas novas e isentas de doenças, materiais, veículos, e ferramentas utilizadas em plantações doentes, efetuar uma poda vigorosa eliminando ramos, gavinhas e frutos doentes, sementeiras e novas plantações deve ser feitas o mais distante possível de áreas de maracujazeiros adultos, as aplicações de fungicidas devem ser realizadas na parte da manhã e não é indicado fazer aplicação em frutos devido a quantidade de resíduos de fungicida que fica no fruto (Ufrgs, 2010).
Dessa forma, o controle dessa doença exige a combinação de várias táticas. O histórico fitossanitários da área de plantio, o histórico do clima da região onde o maracujá vai ser cultivado e a diagnose e o monitoramento da doença são considerados os pilares de sustentação para se iniciar um programa de manejo integrado da cladosporiose. A partir daí deve ser levado em consideração outro aspecto iniciando pelo uso de variedades resistentes e o plantio de mudas sadias (Ufrgs, 2010).
LITERATURA CITADA:
AGROFIT, Disponível em:
CENARGEN, Disponível em:
INDEX FUNGORUM, Disponível em:
KIRK, P. M.; CANNON, P. F.; DAVID, J. C.; STALPERS, J. A.; Dictionary of the Fungi. 9 th Edition, CABI Bioscience. Surrey, UK, 2001.
PIO-RIBEIRO, G.; MARIANO, R. de L.R. Doenças do maracujazeiro. In: KIMATI, H. et al. (Ed.). Manual de fitopatologia: doenças das plantas cultivadas. 3. ed. São Paulo: Agronômica Ceres, 1997. v.2, p.525-534.
UFRGS, Disponível em:
YAMASHIRO, T. Doenças do maracujazeiro. In: RUGGIERO, C. Cultura do maracujazeiro. Jaboticabal: FCAV, 1980. p.94-98.
quarta-feira, 28 de abril de 2010
Aspectos Gerais e Morfológicos do Fungo Colletotrichum sp.
Existem registros por volta de 688 espécies, variedades e formae speciales de fungo pertencente ao gênero Colletotrichum sp. Esse fungos possuem como fase teleomórfica ascomiceto pertencente ao gênero Glomerella sp. A posição taxonômica de Colletotrichum é o Reino Fungi, grupo dos Fungos Mitorpóricos e subgrupo dos Coelomicetos. (INDEX FUNGORUM).
Espécies de Colletotrichum são tradicionalmente diferenciadas com base em caracteres morfológicos e culturais, que devem ser
 considerados simultaneamente e nunca isoladamente. Morfologicamente o fungo apresenta acérvulos circulares, conidióforos simples. Conídios hialinos, ovais a oblongos ou ovais ou falcados. Massa de conídios de coloração rósea, podem estar presentes no acérvulo setas longas, septadas e pigmentadas (GALLI, 1978).
considerados simultaneamente e nunca isoladamente. Morfologicamente o fungo apresenta acérvulos circulares, conidióforos simples. Conídios hialinos, ovais a oblongos ou ovais ou falcados. Massa de conídios de coloração rósea, podem estar presentes no acérvulo setas longas, septadas e pigmentadas (GALLI, 1978).A antracnose em frutíferas é considerada uma doença economicamente importante, ela ataca os ramos novos, folhas, inflorescências e frutos. Nas folhas ha o aparecimento de manchas escuras e de contornos irregulares. As inflorescências afetadas apresentam flores escuras, tomando o aspecto de queimadas pelo fogo, morrendo em seguir. As lesões na ráquis podem levar a queda dos frutos, antes da maturação fisiológica, ou mumificação quando ainda novos. No período de maturação, há o aparecimento de lesões escuras e deprimidas na superfície do fungo, que podem atingir também a polpa. A doença pode ocasionar prejuízos que variam em função do grau de suscetibilidade da planta hospederia e das condições ambientais (SERRA et al. 2008).
A doença que possui como agente causal o fungo pertencente ao gênero Colletotrichum pode ser altamente devastadora, proporcionando perdas de até 100% na produção quando os fatores cultivar suscetível, ambiente favorável ao patógeno e sementes infectadas estiverem simultaneamente presentes durante o período de cultivo (SILVA, 2004). A disseminação de planta a planta se dá principalmente através dos respingos de chuva pois os conídios estão aglutinados por uma substância gelatinosa hidrossolúvel e não são facilmente carregados pelo
 vento. Os conídios uma vez em contato com o hospedeiro, sob condições de umidade, germinam e o promicélio resultante, com prévia formação de apressório, penetra diretamente através da cutícula, pela emissão do tubo de infecção (GALLI et al. 1978).
vento. Os conídios uma vez em contato com o hospedeiro, sob condições de umidade, germinam e o promicélio resultante, com prévia formação de apressório, penetra diretamente através da cutícula, pela emissão do tubo de infecção (GALLI et al. 1978).Entre as medidas de controle desse patógeno, destacam-se: o uso de sementes certificadas, rotação de cultura, controle químico e a resistência genética, sendo esta a mais eficaz, por minimizar os custos de produção e reduzir os danos causados ao ambiente (SILVA, 2004).
Autor: Paulo Vinícius de Sousa
Microbiologia 3º período Agronomia
Referências Bibliográficas:
GALLI, Ferdinando et al, Manual de fitopatologia vol. 2: Doenças das plantas cultivadas. 4. ed. São Paulo: editora Agronômica ceres, 1978.
SILVA, K.J.D. Distribuição e caracterização de isolado de Colletotrichum lindemuthianum no Brasil; Lavras :UFLA, 2004.88.p:il
SERRA, IMRSS...COELHO, R.S.B: MENEZES, M.M. Caracterização fisiológico, patógenica e análise isoenzimática de isolados monospóricos e multiespóricos de Colletotrichum aloeosporoides. Universidade Federal Rural de Pernambuco. UFRPE. Departamento de Agronomia/Fitossanidade. Summa Phytopathol. vol. 34 BOTUCATU Apr./June 2008.
Index fungorum, disponivel em:
acessado em 19 de abril de 2010.
ASPECTOS GERAIS E MORFOLÓGICOS DE Arthrobotrys sp.

O gênero Arthrobotrys sp. foi descrito por Corda, em 1839. Ele pode apresentar as fases anamorfa e teleomorfa. Na fase anamorfa é pertencente ao Reino Fungi, a divisão Hifomicetos, subdivisão dos fungos mitosporicos e apresenta taxonomia insertae sedis (Oliveira, R.D.L. et al., 2002). Na fase teleomorfa ele encontra-se no Reino Fungi, na divisão Ascomycota, subdivisão Orbiliomycetes, classe Orbiliomycetidae, ordem Orbiliales e família Orbiliaceae. Apresenta 13 variedades e 119 espécies registradas (Index Fungorum, 2010).
Este gênero de fungo apresenta conidióforos longos, delgados, simples, septados, hialinos, levemen te alargados no ápice, possui célula conidiogênica simpodial ou irregular, os conídios são hialinos, ovado-oblonga, suportados em denticulo, saprófitas ou parasitas de nematóides (Barnet, H.L. et al., 2000). Quanto aos parasitas de nematóides, produzem extensas ramificações miceliais e, ao longo das hifas, são produzidos os orgãos de captura que prendem os nematóides vivos (Oliveira, R.D.L. et al., 2002).
te alargados no ápice, possui célula conidiogênica simpodial ou irregular, os conídios são hialinos, ovado-oblonga, suportados em denticulo, saprófitas ou parasitas de nematóides (Barnet, H.L. et al., 2000). Quanto aos parasitas de nematóides, produzem extensas ramificações miceliais e, ao longo das hifas, são produzidos os orgãos de captura que prendem os nematóides vivos (Oliveira, R.D.L. et al., 2002).
Cooke (1963) agrupou os fungos predadores de acordo com o crescimento micelial: aqueles que crescem mais rápido são os formadores de redes, seguido dos produtores de nódulos adesivos, e os mais lentos, são os formadores de anéis constritores. Quanto à ocorrência e à distribuição, os numerosos levantamentos têm mostrado que os diferentes grupos de fungos nematófagos são encontrados em todo mundo e nos mais diversos tipos de clima. No Brasil, os estudos com fungos nematófogos encontram-se em sua fase inicial (Oliveira, R.D.L. et al., 2002).
Alguns fungos predadores de nematóide associados às raízes de cana-de-açúcar, apresentam anéis móveis, este grupo se caracteriza por possuir hifas especializadas que formam um verdadeiro anel ou laço que se fecha quando o nematóide toca a parte interna do anel armadilha, imobilizando-o para ser mais tarde colonizado e digerido por hifas apropiadas. Pertencem a este grupo algumas espécies, entre elas Arthrobotrys dactyloides. Mas existem outras espécies que predam com redes adesivas e entre estas estam Arthrobotrys conoides, Arthrobotrys oligospora e Arthrobotrys robusta, neste grupo as hifas especializadas na captura formam uma rede adesiva tridimensional que tem a capacidade de grudar no corpo do nematóide enredando-o para mais tarde ser digerido por hifas apropiadas (Galle, F. et al., 1980).
Diversos antagonistas naturais de nematóides, entre eles, bactérias, vírus, besouros, ácaros e fungos, são descritos como controladores biológicos em potencial, entretanto os fungos nematófagos são os inimigos naturais cujas pesquisas apresentaram melhores resultados no controle de nematóides (Ribeiro, 2003).
Os fungos do gênero Arthrobotrys sp. produzem um extenso sistema de hifas ao longo das quais são produzidas organelas capazes de capturar nematóides (Barron, 1977; Gray, 1987).
Fungos nematófagos vem sendo pesquisados como uma alternativa para control ar diversas espécies de nematóides (Castro et al., 2003) e dentre as espécies de fungos predadores de nematóides que vem sendo utilazadas como agentes controladores biologicos de helmintos gastrintestinais de animais domésticos destaca-se a espécie Arthrobotrys robusta (Araújo et al., 1993, 1998, 1999; Alves et al., 2003; Dimander et al., 2003).
ar diversas espécies de nematóides (Castro et al., 2003) e dentre as espécies de fungos predadores de nematóides que vem sendo utilazadas como agentes controladores biologicos de helmintos gastrintestinais de animais domésticos destaca-se a espécie Arthrobotrys robusta (Araújo et al., 1993, 1998, 1999; Alves et al., 2003; Dimander et al., 2003).
Os nematóides de galha (Meloidogyne spp.) estão entre os principais problemas fitossanitários na produção comercial de olerícolas
Nematóides de galhas (Meloidogyne spp.) provocam queda na produção de hortaliças como o pepino, sendo um fator limitante em áreas infestadas, causando perda do vigor e subdesenvolvimento, deficiência mineral, murcha nas horas mais quentes e baixa qualidade de frutos (Arieira, GO et al., 2009).
A produção de alface em condições de levada temperatura tem sido afetada pelo ataque de nematóides do gênero Meloidogyne. Muitos fungos têm demonstrado capacidade de parasitar fitonematóides, sendo que alguns atuam como parasitas de ovos, como Paecilomyces lilacinus e Arthrobotrys spp. (Paes, VS¹ et al., 2009).
Para se manterem no solo, fungos predadores de nematóides precisam resistir ás flutuações de umidade durante o ano. A velocidade de crescimento e as alterações na cultura fúngica em ambiente com restrição hídrica são indicativos de sua capacidade de sobrevivência. Neste trabalho, utilizou-se a espécie Arthrobotrys conoides (Freire, ES et al., 2009).
LITERATURA CITADA:
OLIVEIRA, R.D.L, FERRAZ, S., ALFENAS, A.C. , DIAS-ARIEIRA, C.R. Caracterização morfológica e isoenzimática de espécies de Arthrobotrys ocorrentes no Brasil. Nematologia Brasileira 26(2):181-197 2002. Disponivel em:<http://docentes.esalq.usp.br/sbn/nbonline/ol%20262/181-197%20pb.pdf>,acessado em 16 de abril de 2010.
INDEX FUNGORUM Disponível em:<http://www.indexfungorum.org/Names/NamesRecord.asp?RecordID=357550>, acessado em 19 de abril de 2010.
INDEX FUNGORUM Disponível em: <http://www,indexfungorm.org/Names/Names.asp>, acessado em 19 de abril de 2010.
Barnet, H.L., Hunter, B.B. Illustrated Genera of Imperfect Fungi, FOURTH EDITION. Disponivel em: <http://arab2000.forumpro.fr >, acessado em 20 de abril de 2010.
Galle, F., Carvalho, P.deC.T.de, Tokeshe, H., Balsamer, E.M.S., Kimate, H.M.S., Cardoso, C.O.N.M.S., Salgado, C.L., Cardoso, E.J.B.N., Filho, A.B. Manual de fitopatologia - Volume 2 - Doenças de plantas cultivadas. Departamento de fitopatologia da Escola Superior de Agricultura “ Luiz de Queiroz “ da Universidade de São Paulo, Piracicaba, S.P., 1980.
Maciel, A.S. Atividade in vitro dos fungos Arthrobotrys robusta, Duddingtonia flagrans e Monacrosporium thausamasium sobre larvas infectantes de Ancylostoma spp. de cães e sua esporulação em meios de cultura. Viçosa : UFV, 2005.Disponivel em:<http://www.tede.ufv.br/tedesimplificado/tde arquivos/8/TDE-2007-01-17T131611Z-233/Publico/texto%20completo.pdr>, acessado em 18 de abril de 2010.
Arieira, G.O.; Santiago, D.C.; Stroze, C.T.; Baida, F.C.; Pereira, R.F.G.; Sbrussi, C.A.G. Universidade Estadual de Londrina, Rod. Celso Garcia Cid Km 380, Londrina, Brasil. Avaliação da eficiência dos biocontroladores de nematóides NEMAT e NEMAPLUS no tratamento de solo em cultivo protegido. Tropical Plant Pathology 34 ( [Suplemento ), S62, agosto 2009.
Paes, V.S., Santiago, D.C., Krzyzanowski, A.A., Takahashi, A., Almeida, V.P., Pontes, A.R., Arieira, G.O., Pereira, R.F.G. UEL, DA, CP 6001, CEP 68051-990, Londrina, PR, Brasil; Laboratorio de Nematologia/APP/IAPAR< style="font-style: italic;"> Arthrobotrys oligospora e Paecilomyces lilacinus no controle de Meloidogyne incognita em alface sob cultivo protegido. XLII Congresso Brasileiro de Fitopatologia, S200, 2009.
Freire, E.S., Campus, V.P., Faria, M., Pinho, R.S.C., Abreu, F.A. Laboratório de Nematologia/Área de Fitopatologia/DFP/UFLA, CP 3037, CEP 37200_000, Lavras, M.G., Brasil. Efeito de resistores hídricos no crescimento de Arthrobotrys conoides in vitro. XLII Congresso Brasileiro de Fitopatologia, S206, 2009.
ASPECTOS GERAIS E MORFOLÓGICOS DO FUNGO Oidium sp.

É uma doença relativamente comum nos anos de inverno seco, mas é raro causar sérios danos à cultura em condições de campo. Entretanto, com o incorreto da plasticultura, é possível que tanto Oidiopsis como Oidium tornem-se patógenos importantes.
Sintomas - Aparecem nas folhas mais velhas em forma de numerosas manchas circulares ou elípticas que, frequentemente, coaslescem, provocando queima e desfolha das plantas com pode ser observado na folha ao lado. Essas manchas são pequenas e variam de 2 a 5 mm de diâmetro, as vezes atigindo até 10 mm, com margem marrom escura, centro cinza, com ou sem hal clorótico. No centro lesão, sob condições de umidade, é possível notar pontos negros contituídos por frutificações do fungo, os picnídios. No caule, pecíolo e sépala , as lesões são, geralmente, menores e mais escuras do que aquelas em folhas. Picnídios podem ou nao estar presentes. As folhas mais velhas sao afetadas primeiro. Posteriormente, os esporos sao disseminados por respingos de água às folhas mais novas maneira semelhante à pinta preta. Os frutos raramente sao afetados.
Controle - As medidas de controle recomendadas para requeima ( Phytophthora infestans ) e pinta preta ( Alternaria solani ), acrescidas de fungicidas sistêmico mais específicos como benomyl, tiofanato metílico, carbendazin e tiabendazol são suficientes para o controle desta doenças.

Descrição Micologica - O fungo Oidium Lycopersici caracteriza - se por apresentar conídios elípticos, hialinos, crescendo em cadeia sobre conidiósforo curtos, não ramificados, produzidos em micélio surpeficial. A absorção dos nutrientes do hospedeiro é feita via haustórios , emitidos pelas hifas septadas e bastante ramificadas. Os conidióforos sao curtos com conídios filiforme,multi-septados e liberados em cirros hialinos, aglutinados por substâncias mucilaginosas.
Autor: Saldanha Bortolott
Microbiologia - Agronomia 3º período
Referências Bibliograficas
Tokeshi, H e Carvalho, P. C. T. Doenças do tomateiro - Lycopersicon esculentum Mill. In: Galli, F Carvalho, P.C.T, Tokeshi, H. Balmer, E, Kimati, H, Cardoso, C.O.N, Balgado, C.L., Krugner, T.L, Cardoso, E.J.B.N., Berganmin Filho, A, . Manual de Fitopatologia, Volume 2 - Doenças das plantas cultivadas. Editora Agronômica ceres, Sao Paulo, SP, 1980
Kurozawa, C e pavan, M.A. Doenças do Tomateiro - Lycopersicon esculentum. In: Kimati, H. , Amorin, L. , Rezende, J.A.M , Bergamin Filho , A. , Camargo, L.E.A , Manual de Fitopatologia, Volume 2 - Volume 2 - Doenças das plantas cultivadas. Editora Agronômica ceres, Sao Paulo, SP,2005.
terça-feira, 27 de abril de 2010
ASPECTOS GERAIS E MORFOLÓGICOS DO FUNGO Glomerella sp.
A classificação dos ascomicetos é baseada nas características morfológicas de suas estruturas de reprodução sexual. O gênero Glomerella sp. está situado na ordem Polystigmatales, juntamente com outros gêneros também de interesse fitopatológico: Phyllachona, Coccostroma e Apiosphaeria (BERGAMIN FILHO, et al. 1978).
DESCRIÇÃO FÚNGICA:
As características do gênero fúngico Glomerella sp. são marcantes e muitas vezes visíveis ao microscópio eletrônico. O gênero Glomerella - Spald & H. Schrenk apresenta a estrutura de frutificação na forma de peritécio do tipo ostiolado, obteliforme (em formato de pêra) e subgloboso. Particulamente, o peritécio pode estar imerso no tecido do hospedeiro simples, superficial ou agregado e algumas vezes com desenvolvimento pobre de clipio ao redor da abertura ostiolar (HANLIN,1997).
 O ostiolo, a abertura por onde saem os ascósporos, é estreito; inconspico; curto; muitas vezes palho, mais palho do que o ascoma; pode ter inúmeros pelos ao seu redor ou pode não ter, sendo classificado como glabro; apresenta várias linhas esteréis internamente do tipo perifece. O ascoma, aprte que abriga as ascas, possui parede do tipo pseudoparenquimatossa; outras células possuem parede fina e pigmentada, finas e hialinas (HANLIN,1997)
O ostiolo, a abertura por onde saem os ascósporos, é estreito; inconspico; curto; muitas vezes palho, mais palho do que o ascoma; pode ter inúmeros pelos ao seu redor ou pode não ter, sendo classificado como glabro; apresenta várias linhas esteréis internamente do tipo perifece. O ascoma, aprte que abriga as ascas, possui parede do tipo pseudoparenquimatossa; outras células possuem parede fina e pigmentada, finas e hialinas (HANLIN,1997) .
.Os ascos são do tipo unitunicados de parede fina, cilíndricos a ligeiramente clavados ou elipsóides; seu ápice não é
amilóide e são sesséis ou curtos. No seu interior pode conter de 4 a 6 ou 8 ascósporos (HANLIN,1997). Os ascos são persistentes, mantendo sua parede após a liberação dos ascósporos, com o ápice contendo um anel estreito (BERGAMIN FILHO, et al. 1978).
Os ascósporos, estruturas sexuais dos ascomicetos, são unicelular; ameroseptados (ausência de septos); sua coloração é clara, portano hialinos; são bisseriados; seu formato é de elipsóide a subcilíndricos; são lisos, curvados e muitas vezes equilaterais, e suas dimensões são menores que 20 micrometros de comprimento (HANLIN,1997).
O habitat característico do gênero Glomerella sp. é parasita ou saprófita de tecidos de plantas vasculares. Possui uma espécie representativa: Glomerella cingulata (Stoneman) Spald & H. Schrenk. A forma anamórfica desse gênero é o Colletotrichum sp. (HANLIN,1997).
Tanto na fase teleomórfica, Glomerella, quanto na fase anamórfica, Colletotrichum, esse gênero fúngico é um importante agente causal do tipo de doença conhecida como Antracnose, que ocorre em muitas plantas. (BERGAMIN FILHO, et al. 1978).
O sintoma morfológico da
 Antracnose é o aparecimento de mancha. Esta doença pode causar morte de plântulas, necrose do pecíolos e manchas nas folhas, hastes e vagens. Em períodos de alta umidade, as paredes infectadas ficam cobertas por pontuações negras, denominadas de acérvulos (ALVES, et al.)
Antracnose é o aparecimento de mancha. Esta doença pode causar morte de plântulas, necrose do pecíolos e manchas nas folhas, hastes e vagens. Em períodos de alta umidade, as paredes infectadas ficam cobertas por pontuações negras, denominadas de acérvulos (ALVES, et al.)Hoje, são válidas em literatura 103 espécies do gênero Glomerella sp. (INDEX FUNGORUM), no Brasil são conhecidos 11 gêneros de Glomerella sp. (EMBRAPA,2010) e ao redor do mundo possui 99 hospedeiras (SBML,2010).
Autora: Bruna Ribeiro Machado
Microbiologia - Agronomia 3º período
REFERÊNCIAS BIBLIOGRÁFICAS:
HANLIN, R.T., Illustrated Genera of Ascomycetes. Volume 1. ed. Apspress. St. Paul, Minnesota, 1997.
BERGAMIN FILHO, A.; KIMATI. H.; AMORIM, L.; Manual de Fitopatologia vol. 1: Princípios e Conceitos, 3ª edição, ed. Ceres, 1995.
INDEX FUNGORUM disponível em:
Acessado em: 26 de abril de 2010
EMBRAPA CENARGEN disponível em:
Acessado em: 26 de abril de 2010
SYSTEMATIC BOTANY OF MYCOLOGICAL RESOURCES disponível em:
Acessado em: 26 de abril de 2010
ALVES, R.C.; DEL PONTE, E.M. Fitopatologia.net - herbário virtual. Departamento de Fitossanidade - Agronomia, UFRGS. Disponível em:
Descrição morfológica Tilletia ayresii
O agente causal do carvão-da-braquiária é o fungo Tilletia ayresii, pertencente ao reino Fungi – de ordem Ustilaginales – da divisão Basidiomicota, família Tilletiacea, e seus principais esporos assexuados são os teliósporos e os sexuados são os basidiósporos, segundo Bergamin (1995).
O carvão da braquiária é uma doença conhecida em várias regiões do Brasil, como nos estados de São Paulo, Minas Gerais, e no sul de Goiás; pois essas regiões oferecem climas e condições favoráveis a esse patógeno. É considerada doença de importância secundária apesar de que possa causar um prejuízo em torno de 10% à 50% na pecuária bovina. (E. J. B. N. Cardoso).
As plantas afetadas espigam um pouco antes que as plantas sadias. Os soros tomam a posição das sementes e estão, inicialmente, recobertos por uma delicada membrana acinzentada que muito cedo se rompe, deixando exposta uma massa de esporos negros e pulverulentos. Em alguns casos, podem aparecer soros nas folhas situadas abaixo da espiga. (E. J. B. N. Cardoso).
No mesmo livro, Bergamin (1995) cita também que este patógeno apresenta especificidade quanto ao hospedeiro, são parasitas evoluídos e obrigatórios. Normalmente desenvolvem micélio monocariótico e dicariótico. Os esporos são facilmente disseminados pelo vento, podendo atingir hospedeiros localizados nas proximidades ou a grandes distâncias da fonte do inóculo.
Os teliósporos são esféricos unicelulares, dicarióticos e após a ocorrência de cariogamia e meiose, germinam, formando um promicélio ou tubo germinativo. Esta estrutura diferencia-se numa basídia septada que por sua vez origina os basidiósporos cilíndricos unicelulares e haplóides. A germinação do basidiósporo da origem à hifa primária. Através do processo de plasmogamia as hifas primárias unem-se aos pares e formam as hifas secundárias que penetram e colonizam os tecidos do hospedeiro, e preferencialmente órgãos florais, o que serve de complemento para o raciocínio de Bergamin (1995).
Os clamidósporos tem um período de viabilidade relativamente curto: alguns meses. Para haver inoculação necessita-se de um período úmido e fresco durante a floração, segundo H, Kimati (1980).
Em todos os casos de carvões aparece grande variabilidade genética, o que implica no aparecimento de raças patogênicas. A existência das raças deve-se em grande parte, ao mecanismo de recombinação genética que ocorre durante o processo de meiose. Bergamin (1995).
As medidas de controle é o emprego de variedades resistentes que, nos países agronomicamente desenvolvidos é um fato bastante corriqueiro. Aqui no Brasil muitas variedades são suscetíveis. Como nesse caso, também é preciso ao se proceder o melhoramento visando conferir a resistência deste patógeno. Existem pelo menos 12 raças fisiológicas no Brasil. (E. J. B. N. Cardoso).
Outro método de controle recomendado é o emprego de sementes sadias, selecionadas de campos isentos de doença, ou de sementes tratadas. O tratamento de semente mais indicado em:
1) Imersão em água a 20-30°C por 4 a 6 horas.
2) Imersão em água a 41-44°C por 1 minuto.
3) Imersão em água de 51-54°C por 10 minutos.
4) Esfriar e secar.
Também é recomendável eliminar as espigas afetadas a fim de diminuir a quantidade de inóculo no campo e a obtenção de sementes certificadas. (E. J. B. N. Cardoso).
A pesquisa feita teve como objetivo realizar uma descrição micológica do fungo Tilletia ayressi,de família, ordem e reino já anteriormente especificados. O trabalho acima apresentado também expõe um pouco mais sobre o grupo de doenças conhecidas como “carvões”, devido a presença de massas pulverulentas de coloração negra encontrada na parte aérea da planta doente.
Foram analisadas no laboratório de Microbiologia do IFGoiano - Campus Urutaí, folhas de braquiária contendo carvões da espécie Tilletia ayresii.
Foi utilizado o método de pescagem direta, que consiste em coleta do material desejado com a ajuda de uma pinça com formato de agulha, e o material coletado é colocado em uma lâmina para estudo e observação do mesmo. Na confecção da lâmina utilizaram-se lamínulas, corante lactofenolcotton-blue e o material coletado. Primeiramente foi colocado o material coletado na lâmina, depois foi aplicado o corante e a fixação da lamínula. A visualização foi feita em seguida, através do microscópio óptico e também com a lupa esterioscópio.
Para visualização futura, foi utilizada uma câmera fotográfica Canon modelo Power Shot A580 para registro. Logo após, utilizou-se esmalte para melhor fixação da lamínula na lâmina, e foi guardada a amostra para estudos posteriores.

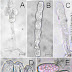
Figura 1. Aspectos morfológicos de Tilletia ayresii. A. panícula produzindo abundante massa escura e enegrecida de teliósporos(bar=150µm), B. Panícula desidratada e chocha, C. teliósporo maduro (escuro) e imaturo (hialino)(bar=45µm), D. teliósporo de parede espessa e superfície irregular(bar=8,5µm).
DESCRIÇÃO MICOLÓGICA
Na figura A apresenta uma panícula produzindo uma massa escura e enegrecida de teliósporos. As doenças causadas por esse fungo ficam conhecidas como carvões devido a presença de massas pulverulentas de panícula desidratada e chocha encontradas na parte aérea de plantas doentes (fig.B) (Index Fungorum).
Os teliósporos são de parede espessa e superfície irregular unicelulares, esféricos, binucleados, podendo apresentar superfície lisa ou ornamentada. São formados a partir do micélio dicariótico, de modo intercalar, a partir da diferenciação das células que compõe as hifas (fig.D). Estas desenvolvem-se normalmente , no interior de partes vegetais originárias de grãos e meristemas modificados. Os basidiósporos são ovalados, unicelulares, uninucleados, hialinos e normalmente não exibem ornamentações (fig. C). Estes esporos são produzidos a partir da germinação do teliósporos. Os basidiósporos podem se multiplicar por brotamento ou podem germinar e produzir um tubo germinativo, que dará origem a uma hifa. O micélio produzido por um basidiósporo é chamado de primário (monocariótico) e não tem capacidade de colonizar os tecidos da planta hospedeira. Em alguns casos dois micélios se unem formando e formam o micélio secundário (Christensen, J.P).
LITERATURA CITADA
BERGAMIN, A.F.; KIMATI, H.; AMORIM, L. Manual de Fitopatologia. 3ª Ed. Ceres: Ave-Maria, 1991.
http://www.zeamays.com.br/doencas/carvoes.htm.
Acesso: 22/06/2010
http://www.canavialis.com.br/newsletter/CanaVialis_Results_Report_6Edicao.pdf.
Acesso: 23/06/2010
CARDOSO, E.J.B.N; Manual de Fitopatologia (Doenças das plantas cultivadas). São Paulo: Agronômica Ceres Ltda., 1980, Vol. 2.
Christensen, J.P; Corn smut caused by Tilletia ayressi. American Phytopathologycal Society 2: 1963.
ASPECTOS GERAIS E MORFOLÓGICOS D\O FUNGO Puccinia polysora (Paulo R.)
O fungo Puccinia polysora pertencente à divisão basidiomicota, classe teliomicetes, ordem uredinales, família pucciniaceae, é o agente causal da ferrugem polysora, doença incidente e importante para a cultura do milho (Fantin & Duarte et al., 2009) .
A família Pucciniaceae encontra-se dentro da ordem Uredinales, classe Teliomycetes e Divisão Basidiomycota, apresentando como principais gêneros Puccinia sp. e Uromyces sp. importantes fungos causadores de doenças em cultivos agrícolas. Estes patógenos obrigatórios causam danos em diversas plantas cultivadas e selvagens, em praticamente todos os continentes, causando sérias perdas em plantios comerciais por interferir com a fisiologia do hospedeiro, reduzindo a produtividade e depreciando os produtos agrícolas (CUMMINS & HIRATSUKA et al., 1983;).
O gênero Puccinia sp. possui em torno de 4.000 espécies em vários hospedeiros(Hawksworth et al., 1995). Pers., Neues MagPucciniaceae, Pucciniales, Incertae sedis, Pucciniomycetes, Basidiomycota, Fungi. Bot. 1: 118 (1794)Underw. 1897, polysora Pucciniaceae Underw., Bull. bot Torrey. Club 24: 86 Sinonímia (1897): Dicaeoma polysorum (Underw.) Arthur (1906Synonymy) Contribuinte (s): IMI (2008)(Index Fungorum, 2010).
Existem 12 tipos de espécies de ferrugens incidentes em milho(Zea mays):
Angiopsora zeae, Phakopsora zeae, Physopella zeae, Puccinia maydis, Puccinia pallescens, Puccinia polysora, Puccinia purpúrea, Puccinia sorghi, Puccinia polysora, Uredendo zeae, Uredo pallida, Puccinia SP(ntars-grin fungaldatabases, 2010).
A ferrugem polissora, causada pelo fungo Puccinia polysora é considerada a mais destrutiva das ferrugens que afetam a cultura do milho. Tem sido relatada em muitas áreas tropicais e subtropicais do mundo onde se cultiva o milho (Melching et al., 1975; Shurtleff et al., 1992;) e é particularmente bem adaptada a ambientes onde prevalecem temperatura e umidade elevadas. P. polysora tem sido considerada de grande importância nas regiões tropicais do Brasil, predominando em regiões abaixo de 700 metros de altitude em
• semeadura a partir de outubro. Em regiões mais altas, a doença pode ocorrer com maior intensidade geralmente apenas em plantios iniciados a partir de dezembro (Silva et al., 1997;). De acordo com estudos realizados pela Embrapa, no Brasil são conhecidas as seguintes ocorrências de ferrugens:
• Tripsacum australe Cutler & E. Anders. (Poaceae) ARQUIVOS DO INSTITUTO BIOLÓGICO 49(Supl.):82, 1982 Ferrugem PA.
• Tripsacum laxum Nash (Poaceae) ARQUIVOS DO INSTITUTO BIOLÓGICO 49(Supl.):82, 1982 Ferrugem RJ.
• Tripsacum sp. L. (Poaceae) ARQUIVOS DO INSTITUTO BIOLÓGICO 49(Supl.):82, 1982 Ferrugem PA, RS.
• Zea mays Linn. (Poaceae) [ MILHO ] FITOPATOLOGIA BRASILEIRA 23(Supl.):230, 1998 Ferrugem polisora Ocorre em sementes MG, ES, GO, MS, MT, PR, RJ, RS, SC, SP, PE, PB, DF, PA( Fungos, Cenargem, 2010).
Esta ferrugem pode causar rápida necrose na planta, ocorre durante todo ano agrícola, constituindo-se problema importante em plantios a partir da segunda quinzena de novembro. P. polysora tem preferência por temperaturas mais elevadas e é menos exigente em relação à umidade para germinar, a severidade da ferrugem-polysora é favorecida por umidade relativa alta e temperaturas em torno de 27°C, em condições favoráveis o fungo P. polysora, produz grande quantidade de inóculo e há extensiva disseminação dos esporos do patógeno pelo vento (Fantin & Duarte et al., 2009).
A ferrugem-polysora, pode ser observada inicialmente nas folhas baixeiras, na forma de pústulas circulares e ovais, marrom claras, distríbuídas na face superior das folhas e com muito menos incidência na face inferior da folha. Nestas, as pústulas são produzidos os urediniósporos que quando expostos, dão de aspecto pulverulento e ferruginoso característico das plantas, os teliosporos são raros e normalmente não germinam, sendo de pouca importância no ciclo da doença. As folhas infectadas geralmente amarelecem e secam em pouco tempo pela intensa queima foliar (Fantin & Duarte et al., 2009).
As ferrugens são pleomórficas podendo apresentar vários tipos de estruturas esporogênicas e esporos com diferentes morfologias e funções, produzidas nos diversos estágios ou fases de seus ciclos vitais, por vezes extremamente complicados e confusos. Em virtude de algumas espécies poderem apresentar até cinco tipos de esporos diferentes (ou raramente,
até mesmo seis, como é o caso de Puccinia vexans, as ferrugens estão entre os microrganismos de ciclo biológico mais complexo (CUMMINS, 1959; CUMMINS; HIRATSUKA, 1983).Entretanto, muitas ferrugens, mesmo pertencendo ao grupo que requer dois hospedeiros diferentes para seu ciclo completo, podem sobreviver em um único hospedeiro por meio de reprodução vegetativa ou clonal (urediniosporos) que é caso da ferrugem-polissora. No caso das ferrugens denominadas autoécias, em que todos os estados esporíferos manifestam-se em um mesmo hospedeiro, a determinação dos ciclos de vida deveria ser mais simples, não fosse a grande variabilidade existente em certas espécies.
Mais de 11raças deste patógeno já foram descritas e evidências de novas raças têm sido observadas nos últimos anos no Brasil Central e até o momento não são conhecidos hospedeiros alternativos deste patógeno (Kimati et al., 2005).
O objetivo deste trabalho é apresentar os aspectos gerais e morfológicos do fungo Puccinia polysora.
Folhas de milho (1051 AGROCERES), plantado em 20-01-10, coletadas na cidade de Ipameri-GO, Vila Estrela, Rua Inhambi n°2, lote 2, foram analisadas no laboratório de microbiologia do IFG campus Urutaí.
Utilizando o método de “pescagem direta” com uma pinça em formato de agulha e o método de corte histológico foi possível preparo de lâminas semi permanentes. Visualizou-se através do microscópio ótico e iniciou-se os procedimentos de descrição e registro microfotográfico.
Nestas lâminas foram depositadas duas gotas de fixador lacto fenol cotton-blue, sendo logo após depositado uma lamínula e depois passou-se esmalte sobre estas para melhor fixação.
Figura 1. Aspectos morfológicos do fungo Puccinia polysora, A. Representação dos sintomas, pústulas presentes na folha e no colmo(com melhor representação)(bar=189µm), B. Intensa queima foliar (Outro sintoma observado num estágio mais avançado da doença), C. Representação dos urediniósporos de coloração variada(amarelo a dourado)(bar=189µm), D. Urediniósporos em estágio maduro(escuros) e Imaturos(claros)(bar=47,25µm), E. Urediniósporos de parede espessa com dois poros germinativos(bar=9,45µm), F. Foto do corte, urédias, que rompem a epiderme.
Descrição Micológica
As pústulas formadas são predominantemente circulares, de cor marrom-clara em plantas jovens, e tornam-se marrom-escuras à medida em que a planta se aproxima da fase de maturação(fig. 1A). Essas pústulas encontram-se densamente distribuídas em ambas as faces das folhas e podem ser normalmente observadas ainda cobertas pela epiderme. Aquelas que já romperam a epiderme apresentam aspecto pulverulento(urédias)(fig.1F)(Fitopatologia UESB., 2010). A intensa queima foliar é um sintoma observado num estágio mais avançado da doença(fig.1B).
O fungo Puccinia polysora possui urediniósporos caracteristicamente ovais e irregulares, binucleados de cor amarelada(fig. 1E), e apresentam poros germinativos de posição equatorial (fig.1E). Os urediniosporos são unicelulares sendo suas superfícies usualmente ornamentadas delicadamente, equinuladas, ou verrugosas de forma uniforme ou não. A posição e o número de poros germinativos presentes nos urediniosporos são razoavelmente constantes para uma determinada espécie Quanto a posição nos esporos, os poros germinativos estão em posição equatorial(fig.1E(Arq. Inst. Biol., 2008)).
Referências Bibliográficas
Arquivos do Instituto Biológico, v.75, 2008 São Paulo, p.117-134.
CUMMINS, G.B.; HIRATSUKA, Y. Illustrated genera rust fungi. St. Paul: American Phytopathological Society, 1983. 152p.
EMBRAPA, Cultivo do Milho, Doenças Foliares. Disponível em:http://sistemasdeproducao.cnptia.embrapa.br/FontesHTML/Milho/CultivodoMilho_2ed/doencasfoliares.htm Acessado em 12 de abril de 2010.
FANTIN, G.M.; SILVA, H.P.; BALMER, E.; MIRANDA FILHO, J.B. de. Herança da resistência à ferrugem causada por Puccinia polysora em milho. Fitopatologia Brasileira, v.18, p.332-333, 1993.
Fantin G.M., Duarte A.P, Manejo de doenças na cultura do milho safrinha. Campinas, Instituto Agronômico. 2009, p.16, 17, 18, 19.
Ferrugem em espécies de zea, Disponível em http://nt.ars-grin.gov/fungaldatabases/ acessado em 24 de junho de 2010.
Fitopatologia, Universidade Estadual do Sudoeste Bahia. Disponível emhttp://www.uesb.br/utilitarios/modelos/monta.asp?site=fitopatologia&tex=iii_10_milho.html Acessado em 12 de abril de 2010.
Fungos, Puccinia Polysora, Cenargem, Embrapa. Disponível em http://pragawall.cenargen.embrapa.br/aiqweb/michtml/fichafg.asp?id=3507 acessado em 30 de junho de 2010.
Index Fungorum, Puccinia polysora. Disponível em http://www.indexfungorum.org/names/Names.asp Acessado em 23 de junho de 2010.
KIMATI H., AMORIM L, REZENDE J.A.M., BERGAMIN FILHO A, CAMARGO, L.E.A. CAMARGO. Manual de fitopatologia/edição de hiroshi Kimati. [et.al.]-4ed.-,São Paulo;Agronômica Ceres.2005.2v.:IL p.479.
MELCHING, J.S. Corn rusts: types, races and destructive potencial. In: ANNUAL CORN AND SORGHUM RESEARCH CONFERENCE, 30., Washington, 1975. Washington: American Seed Trade Association, 1975. p.90-115.
SHURTLEFF, M.C. (Ed.) Compendium of corn diseases. 2.ed. St. Paul: American Psychopathological Press, 1992.105p.
Hawksworth, D. L, P. M. Kirk. B. C. Sutton & D. N. Pegler.1995. Ainsworth & Bisby’s Dictionary of the fungi. CAB International, Cambridge, Univ. Press.
ASPECTOS MORFOLOGICOS DO FUNGO Colletotrichum gloesporioides.
.jpg)
O Fungo Colletotrichum gloesporioides foi encontrado em folhas de mandioca onde é causador da antracnose. A antracnose da mandioca ocorre em vários países produtores. No Brasil, a doença esta presente em todas as regiões produtoras, porem é mais severa no Nordeste e no Sudeste, onde as condições ambientais são mais favoráveis à sua ocorrência.
Existem basicamente dois tipos de antracnose em nossas condições, a branda e a severa. A forma branda normalmente afeta plantas no final do ciclo e é causada por estirpes fracas do patógeno. A forma severa, causada por estirpes mais agressivas, provoca danos maiores, principalmente se o ataque ocorrer em cultivos com menos de quatro meses. Não existem dados de perda na produção. Variedades suscetíveis infectadas na fase jovem são severamente afetadas, podendo ocorrer à morte de toda a parte aérea da planta.
Sintomas – Sintomas característicos aparecem na forma de cancros elípticos e profundos nas hastes jovens e pecíolos. Sob condições de alta umidade, observa-se no centro destas lesões uma massa de coloração rósea, constituída por esporos do fungo. Em decorrência desta infecção, a planta desfolha e os ponteiros morrem. Esporadicamente pode ocorrer morte total da parte aérea. O plantio de manivas contaminadas pode resultar em falhas na germinação e conseqüente redução no numero de plantas por área.
Etiologia – O fungo C.gleosporiodes corresponde à forma imperfeita de Glomerella cingulata, q.jpg) ue inclui numerosas formae speciales. A viabilidade patogênica do fungo pode estar associada com a presença do ciclo sexual, que representa uma possibilidade de recombinação genética.
ue inclui numerosas formae speciales. A viabilidade patogênica do fungo pode estar associada com a presença do ciclo sexual, que representa uma possibilidade de recombinação genética.
As condições favoráveis à ocorrência da doença são períodos longos de chuva com temperaturas entre
Controle – Deve-se evitar o plantio de variedades sabidamente suscetíveis em locais de condições climáticas favoráveis à ocorrência da doença. Alem disso, medidas complementares que se baseiam na redução do inoculo devem ser consideradas, como: a) seleção de manivas sadias para plantio; b) imersão das manivas por 5 minutos em solução de benzimidazol (100 g/100 L água ); c) poda e eliminação de gastes afetadas.
BIBLIOGRAFIA
- MASSOLA JUNIOR, N.S.; BEDENDO, I. P. Doenças da mandioca. p. 449. In: Edição de KIMATI, H.; AMORIM, L.; REZENDE, J. A. M.; BERGAMIN FILHO, A.; CAMARGO, L.E.A. Manual de fitopatologia - Volume 2 - Doenças das plantas cultivadas. 4. ed. São Paulo: Agronomica Ceres, 2005. p.663.
segunda-feira, 26 de abril de 2010
Sclerotinia sclerotiorum (MOFO BRANCO DA SOJA)

Sclerotinia sclerotiorum (MOFO BRANCO DA SOJA)
A podridão branca da haste esta disseminadas por todas as regiões de condições climáticas amenas (Região Sul e chapadas dos cerrados, acima de 800 m de altitude). Alem da soja, o fungo infecta uma vasta gama de plantas cultivadas e daninhas, com exceção das gramíneas. A fase mais vulnerável vai do estádio da floração plena (R2 ) ao inicio da formação das vagens (R3/R4). O fungo é capaz de infectar qualquer parte da planta, porem, as infecções iniciam-se com mais freqüência a partir das inflorescências e das axilas das folhas e ramos laterais.
Referências bibliográficas
KIMATI, H.; AMORIM, L.; REZENDE, J.A.M.; BERGAMIN FILHO, A.; CAMARGO, L.E.A.; Manual de fitopatologia: Doenças das plantas cultivadas. 4ª Ed. Vol. 2, pag. 580 – São Paulo: Agronômica Ceres, 2005.
quinta-feira, 22 de abril de 2010
"ASPECTOS GERAIS E MORFOLOGICOS DO FUNGO Aspergillus flavus"

Figura 1. Aspectos morfológicos de Aspergillus flavus. A. O crescimento do fungo em uma superfécie, observa-se sua estruturas, B. conidióforo (cf) jovem e maduro de cor hialina, C. conidióforo (cf) com célula ampuliforme (ca) e células conidiogênicas (cc), D. três camadas de células conidiogênicas (cc) ligadas a célula ampuliforme (ca), E. conídios (con) esféricos, ameroseptados e hialinos.
DESCRIÇÃO MICOLOGICA
O fundo apresenta conidióforo hialino (Figura 1B), bem desmvolvido, com abundante produção de conódios. A última célula do conidióforo possui uma formato ampuliforme, no qual dezenas de fiálides (Figura 1D) emergem para prdução de conídios. Os conídios esféricos (Figura 1E,D), ameroseptados, e hialinos são produzidos em cadeias. A célula ampuliforme que sustenta as fiálides quando jovem e globosa de cor clara e não pulverulenta (Figura 1D). Fungos pertencentes a este grupo estão por toda parte, e em sementes, podem ocasionar deterioração do embrião impedindo consequentemente a germinação.
REFERENCIAS BIBLIOGRAFICAS
VIDATO, V. Micologia Médica. São Paulo, 2004.
WIKIPEDIA. Disponível em: <http://en.wikipedia.org/wiki/Aspergillus> Acesso em: abril de 2010.
ADAM SERTAOGGI. Disponível em: <http://adam.sertaoggi.com.br/encyclopedia/ency/article/001326.htm> Acesso em : abril de 2010.
BIS BRASIL INDUSTRIAL SOLUTIONS. Conheça a aflatoxina B1. Disponível em:
Seguidores
Postagens populares da Ultima Semana
-
Um grupo parafilético, em biologia, é um grupo de organismos que inclui um ancestral comum e alguns, mas não todos, os seus descendentes. E...
-
1. INTRODUÇÃO De acordo com Alves (1985), a bananeira é de origem do sudeste asiático , podendo ser encontrada, n...
-
1. INTRODUÇÃO A exploração da manga ( Mangifera indica - anacardiaceae) no Brasil, historicamente, foi feita em moldes extensivos...
-
Marcus Vinícius Santana Acadêmico do curso de Agronomia 1 INTRODUÇÃO O maracujazeiro é uma planta tropical originária da América Tropica...
-
ASPECTOS GERAIS E MORFOLÓGICOS DE Oidium sp. Janaina Graziele de Oliveira Lopes e Milton L. Paz-Lima Acadêmica do Curso de Agronomia Profess...
Links de Busca
- Arquivos do Instituto Biológico
- British Library
- Busca de Artigos Science Direct
- CBS Knaw, Utrech Netherlands
- CORE banco de dados
- Defesa Vegetal
- Doenças causadas por Fungos em Plantas do Brasil
- Doenças em Plantas no Japão
- Doenças em Plantas nos EUA - Farr e Rossman
- European journal of Phytopathology
- Horticultura Brasileira
- Indiana University
- Indice de Nomenclatura de Fungos
- Indice de Nomenclatura de Nematóides
- Indice de Nomenclatura de Plantas
- Indice de Nomenclatura de Virus
- Indice para Nomenclatura de Bactérias
- Info Praga Cenargen
- Journal of Phytopathology
- Micologia
- Mycobank
- Mycoscience
- NCBI - pesquisa
- Nematóides em Plantas do Brasil
- PAB Pesquisa Agropecuária Brasileira
- Plant Disease-Phytopathology-Plant Microbe-APS Net
- Q-Bank
- Revista Cientifica: Studies in Mycology
- Revista de Agricultura Neotropical
- Revista Tropical Plant Pathology
- Serviço do Departamento de Agricultura norte-americano com todo tipo de informação relacionada a agricultura.
- Sociedade Britânica de Micologia
- Summa Phytopathologica
- University of California