Mancha-aveludada da
pimenta-malagueta (Capsicum frutescens) causada por Phaeoramularia capsicicola
Álvaro de Oliveira Cardoso
Acadêmico do curso de Agronomia
INTRODUÇÃO
A pimenta-malagueta (Capsicum frutescens), Solanaceae, é um arbusto pequeno, nativo de regiões
tropicais da América, muito cultivado no Brasil, de folhas ovais, acuminadas,
flores alvas e bagas fusiformes, vermelhas, bastante picantes. É usada como
condimento e tempero nas regiões do Brasil, nos estados de Goiás e Minas Gerais
(REIS, 2010).
A “malaguetinha-caipira” destaca-se
pela alta concentração da capsaicina e baixíssimos teores de piperina. Geralmente as variedades comercializadas,
via de regra, são espécies
híbridas, resultantes de cruzamentos realizados para desenvolver variedades
mais produtivas, mais resistentes a pragas e menos atrativas aos pássaros e insetos (MONTEIRO, 2000.)
Por conter vitaminas A, C, do complexo B, potássio e
cálcio, a pimenta pode ser benéfica não somente à saúde do coração, como também
ao sistema circulatório. Apresenta propriedades vasodilatadoras, impedindo a
formação de coágulos e aumentando o calibre de vasos sanguíneos, fatores que
reduzem as chances de um ataque cardíaco ou acidente vascular cerebral. (MENDES, 2013).
É uma cultura que exige
temperaturas elevadas, em torno de 25 a 30°C, durante todo o ciclo de vida. Não
é resistente à baixas temperaturas e intolerante à geadas, onde sua germinação
é reduzida, crescimento reduzido e estiolamento de folhas. Em regiões que
apresentam inverno ameno, principalmente em baixa altitude, a semeadura pode ser
feita durante o ano todo. (PINTO et al., 2007).
Em 2004, foram comercializadas,
nas Ceasas de Minas Gerais, cerca de 270 t de pimenta, ao preço médio de R$
2,99/kg. Deste total, 2,31% foram provenientes do estado de São Paulo e o
restante produzido em Minas Gerais. (PINTO et al., 2007).
A mancha-aveludada tem como agente
causal fungos do gênero Phaeoramularia sp.
Vassiljevsky, são parasitas obrigatórios de um
grande número de espécies de plantas da família das solanáceas. Dentro do
gênero Phaeoramularia, apenas uma espécie é encontrada nos sistemas de produção
agrícola de pimenta e pimentão, as quais têm ampla gama de hospedeiros e podem
parasitar praticamente todos os indivíduos do gênero Capsicum sp. (TRAZILBO
JÚNIOR et al., 2007).
O sintoma mais visível do ataque
da mancha-aveludada são manchas com aspecto aveludado, principalmente na face
inferior da folha, as quais apresentam comumente áreas cloróticas. As folhas
infectadas são geralmente mais curtas e com menor desenvolvimento, justamente pela área da mancha consumida pela
doença. (MOREIRA, 2007).
O
patógeno apresenta ampla distribuição mundial, ocorrendo geralmente em países
de clima tropical e/ou próximos à linha do Equador. Sua necessidade de climas
quentes com temperaturas entre
23-27 °C e umidade relativa superior a 90 % o torna intolerante à climas amenos
e temperados (PINTO et al., 2007).
DESENVOLVIMENTO
Hospedeiro/cultura: Pimenta (Capsicum frutescens L.)
Família Botânica: Solanaceae
Doença: Mancha-aveludada
Agente Causal: Phaeoramularia capsicicola Vassiljevsky
Local de Coleta: Urutaí, GO.
Data de Coleta: 24/02/15
Taxonomia: A fase telemórfica pertence ao reino Fungi,
filo Ascomycota, classe Dothideomycetes, ordem Capnodiales,
família Mycosphaerellaceae. A fase
anamórfica pertence ao Reino Fungi, Grupo inserto dos Fungos Mitospóricos,
sub-grupo dos Hifomicetos, gênero Phaeoramularia sp., espécie Phaeoramularia capsicicola (INDEX FUNGORUM, 2015)
SINTOMATOLOGIA:
Os
sintomas da doença ocorrem principalmente nas folhas, que apresentam inicialmente,
lesões aquosas translúcidas, de coloração verde-escura. Com o desenvolvimento
da doença, as lesões tornam-se branca-acizentadas, de formato circular,
apresentando anéis concêntricos, com bordos escuros e centro cinza-claro. As
lesões podem coalescer, formando grandes áreas necróticas, que se desprendem
das folhas. Sob condições ambientais favoráveis, pode ocorrer intensa desfolha,
que favorece a exposição dos frutos diretamente a luz solar, bem como, ao
ataque de organismos secundários. Os sintomas podem também ser observados no
caule, ramos e pedúnculos dos frutos onde as lesões tendem a ser maiores e mais
alongadas (LOPES e ÁVILA, 2003).
No
campo observa-se claramente a mancha-aveludada nas folhas das plantas, declínio
vagaroso, queda prematura das folhas, queda na produção. Dentre os danos
causados ao sistema aéreo incluem-se a formação de manchas que apresentam
comumente áreas cloróticas que chegam a causar necrose na parte abaxial da
folha, podendo levar à diminuição da parte aérea, e consequentemente por
prejudicar a área de realização fotossintética, também influencia sobre a
produtividade da pimenteira (TRAZILBO JÚNIOR, et al., 2007).
As manchas provocadas pelo fungo
abrigam conidióforos e conídios, e tem cerca de 1,5 cm de largura, e muitas
vezes são circundadas por um halo alaranjado. Quando as infecções são muito severas,
geralmente tem manchas sub orbiculares de coloração marrom bem visíveis,
presente em ambas as superfícies (DEITGHTON,
1976).
ETIOLOGIA:
O conidióforo
é hipófilo, possui colônias anfígenas, conídios fasciculados, de cor marrom
meio pálido ou marrom oliváceo, medindo 22 a 62 µm de comprimento por 4 a 6 µm
de largura. Possui conídios hialinos com cicatrizes de secessão com 1 a 5
µm de diâmetro, filiformes com 2 a 4 septos, medindo 12 a 92 µm de comprimento
por 3 a 7 µm de largura (DEITGHTON, 1976).
O
micélio pode apresentar hifas coloridas e apresenta de 2-3 µm de espessura. O estroma, tecido
fúngico é sub estomático
que varia de tamanho, podendo ter de 35 x 25 µm compostos por hifas de
coloração palha à olivácea (DEITGHTON, 1976).
Tabela 1. Comparação de características morfológicas e morfométricas
de Phaeoramularia capsicicola com o isolado descrito por Deitghton
(1976).
|
Características
|
Isolado Urutaí (2015)
|
Deitghton (1976)
|
|
Dimensões do conidióforo (µm)
|
23,7 x 15,91
|
22-62 x 4-6
|
|
Dimensões dos conídios (µm)
|
38,23 x 0,76
|
12-92 x 3-7
|
|
Número de septos do conídios
|
4
|
2-4
|
|
Forma do conídio
|
Filiforme
|
Filiforme
|
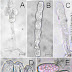
Figura
1. Sintomas e sinais da mancha-aveludada
da pimenta-malagueta (Capsicum frutescens) causada por Phaeoramularia capsicicola. A. lesões irregulares e enegrecidas da face
adaxial (bar = 4 mm), B. detalhe da lesão enegrecida (bar = 2 mm), C.
agrupamento de conidióforos do tipo esporodoquial (bar = 5,94 µm), D. conídios
filiforme curto, E. conídio, alongado e septado, e1. septação, F.
conídio multisseptado, f1. cicatriz
de secessão conidial (bar = 1,4 µm ).
EPIDEMIOLOGIA:
O fungo da
mancha-aveludada tem-se no
Brasil apenas um registro de ocorrência segundo
o Banco de dados da Embrapa Recursos
Genéticos e Biotecnologia, que aponta o estado de SP e
indica Capsicum frutescens Willd (Solanaceae)
a pimenta-malagueta como hospedeira (HINO
et al., 1978).
A
doença incide sobre Capsicum annuum,
e é um fungo de presente em regiões
tropicais e subtropicais. Já foi descrito na Espanha, Bulgária, Romênia,
Marrocos, Etiópia, Uganda, Sudão, Quênia, Tanzânia, Malawi, Zaire, Zâmbia,
Rodésia, Nigéria, Gana, Serra Leoa, Ilhas Maurício, Índia, Nepal, Burma, Sabat,
Trinidad e Tobago, Jamaica, El Salvador, Brasil, Venezuela, Argentina e Estados
Unidos (DEITGHTON, 1976).
O fungo sobrevive nos restos da cultura deixados no campo na forma de
micélio e conídios; também sobrevive nas sementes contaminadas superficialmente
(AGROFIT, 2010). Tão quanto, um dos métodos de controle, cultural, é justamente
eliminar restos culturais de pimenta e pimentão, os quais são propícios para a
conservação de estruturas de sobrevivência do fungo.
A disseminação a longa distância pode ocorrer pelas sementes
contaminadas, porém esta via não é muito comum. Os conídios no campo são
disseminados pelo vento e respingos da água da chuva ou da irrigação por
aspersão. Trabalhadores, insetos, implementos e pássaros também contribuem para
a disseminação do fungo, pois em contato com a planta que foi infectada com o
patógeno, este possuirá a fonte de inóculo em seu corpo, que em contato com uma
planta sadia, iniciará o processo de infecção, onde os esporos germinam em até
48 horas em condições de umidade e temperaturas ideais (SILVA, 2010).
Temperaturas entre
23-27 °C, umidade relativa superior a 90 % e solos de baixa fertilidade são
condições que favorecem o desenvolvimento da doença (AGROFIT, 2015).
CONTROLE:
O controle se baseia em plantar sementes de boa qualidade, adquirida de
firmas idôneas, ou mudas comprovadamente sadias; Evitar o plantio próximo a
culturas velhas; Adubar corretamente a plantação, com base na análise de solo;
Fazer um bom manejo de irrigação, evitando aplicar excesso de água; Evitar
plantios em épocas com alta intensidade de chuva, especialmente quando a
temperatura for alta; Eliminar os restos de cultura logo após a última
colheita; Fazer rotação de culturas (geralmente com gramíneas) por, pelo menos,
um ano (LOPES e ÁVILA, 2003).
O controle físico pode ser feito no manejo de irrigação, caso seja em
ambiente controlado, é prudente que as folhas das pimenteiras não sejam
molhadas, o que é muito difícil no caso da aspersão. Entretanto, este método de
controle acaba sendo preventivo (PINTO et al., 2007). Não há nenhum produto registrado para
controle do patógeno sobre o hospedeiro do boletim, e também não
há registros de controle genético e biológico para essa cultura (AGROFIT, 2015).
LITERATURA CITADA:
DEITGHTON, F.C Brown leaf
mould os Capsicum caused by Phaeoramularia capsicicola. Transiction
British Mycological 67 (1):140 – 142 1976.
FARR, D.F., e ROSSMAN, A.Y. Fungal Databases, Systematic Mycology and
Microbiology Laboratory, ARS, USDA. Disponivel em: < http://nt.ars-grin.gov/fungaldatabases/fungushost/FungusHost.cfm>,
acessado em julho de 2015.
LOPES, C.A. e ÁVILA, A.C. Doenças do pimentão:
diagnose e controle. Brasília: Embrapa Hortaliças, 2003.
MATSUOKA, K.; VANETTI, C.A.; COSTA, H.; PINTO, C.M.F. Doenças causadas por fungos em pimentão e pimenta. Informe Agropecuário, Belo Horizonte, v.18, n.184, p.64-66, 1996.
MENDES, M.A.S.; URBEN, A.F.; Fungos relatados em plantas no Brasil, Laboratório de Quarentena Vegetal. Brasília, DF: Embrapa Recursos Genéticos e Biotecnologia. Acessado em: 26/05/2015.
Ministério da Agricultura, Pecuária e Abastecimento -
Coordenação-Geral de Agrotóxicos e Afins/DFIA/DAS. Disponível em:
http://agrofit.agricultura.gov.br/agrofit_cons/principal_agrofit_cons. Acesso em 12/5/2015.
MONTEIRO, A.J.A.;
COSTA, H.; ZAMBOLIM, L. Doenças causadas por fungos e bactérias em pimentão e
pimenta. In: ZAMBOLIM, L.; VALE, F.X.R.; COSTA, H. (Ed.) Controle de
doenças de plantas: hortaliças. Viçosa: Universidade Federal de Viçosa, 2000.
v.2, p.637-675.
SILVA, C.R. Mancha preta causada por Cercospora capsici em folhas de Pimentão (Capsicum annuum).
Disponível em:
http://fitopatologia1.blogspot.com.br/2010/04/mancha-preta-causada-por-cercospora.html
Acessado em: 18 de abril de 2010.
TRAZILBO JÚNIOR, P.J.; VENZON, M. 101 Culturas, Manual de tecnologias agrícolas.
Belo Horizonte: Empresa de Pesquisa Agropecuária de Minas Gerais, v.2, p.
625-632. 2007.