Está doença é também chamada de podridão-do-colo e está distribuída em regiões de clima tropical e subtropical, em locais onde ocorrem temperaturas altas e umidade seguida de períodos de seca. O agente causal afeta um grande número de hospedeiros em diversos gêneros de plantas cultivadas e silvestres (Bianchini et al., 2005).
Esta doença ocorre de forma generalizada em todo o Brasil, atingindo, além do feijão, diversos cultivos de grande importância econômica. Embora bastante disseminada, a doença geralmente não ocasiona prejuízos elevados, pois o patógeno depende fundamentalmente das condições favoráveis para o seu desenvolvimento (Alves e Del Ponte, 2010).
Punja (1985), o fungo também pode causar tombamento, podridão radicular e murcha em mais de 500 espécies de plantas, é ocasionalmente encontrado em algodão. Primeiramente observado em tomate na Florida em 1892, tem sido regularmente reportado causando podridão na raiz e colo da planta em tomate. Segundo Mendes (2010), a doença pode ser encontrada nas diversas espécies e famílias como no pimentão, amendoim, beterraba, soja, milho, arroz, trigo, cevada, girassol, alface, couve-flor, cebola, quiabo, alho, Anacardiáceae, diversas Cucurbitáceas e muitos outros hospedeiros. Perdas significativas ocorrem em solos infestados pelo patógeno e que apresentam textura leve e umidade próxima à capacidade de campo (Punja, 1985). No sul dos EUA as perdas podem atingir 5 % da produção anual. No Brasil, desconhecesse a magnitude destas perdas. Os sintomas iniciam-se com lesões marrons e aquosas sobre o colo. As lesões avançam, produzindo escurecimento e podridão do caule, resultando em destruição do córtex e da raiz principal. Conseqüentemente, na parte aérea os sintomas são de amarelecimento das folhas inferiores, e conseqüentemente nas folhas superiores. As plantas severamente afetadas apresentam estrangulamento do colo, o que provoca murcha da parte aérea, seca, queda de folhas e morte da planta (Cardoso, 1994).
Segundo Mendes (2010), no Brasil a doença é encontrada na seguinte região e estados como NE, MG, PE, SP, DF, BA, SC, TO, ES, PB, RS. Sendo registradas atualmente aproximadamente 464 espécies de Sclerotium (Index Fungorum, 2010).
Segundo Farr e Rossman (2010), é encontrado o S. rolfsii em vários países do mundo, sendo os principais países com maior incidência da doença em espécies hospedeiras os EUA, Brasil, Austrália, China, Venezuela e dentre outros países do mundo, ocorrendo em aproximadamente 733 espécies de plantas hospedeiras, sendo as principais Allium cepa L., Arachis hypogaea L., Capsicum frutescens L., Daucus carota L., Delphinium sp., Glycine Max L., Ipomoea batatas L., Lycopersicon esculentum Mill, Nicotiana tabacum L., Oryza sativa L., Phaseolus vulgaris L., Saccharum officinarum L., Solanum tuberosum L., Zea mays L.
A infecção das plantas pelo fungo em qualquer estádio do seu desenvolvimento compromete seriamente a produção. Na Região Centro-Oeste, este fungo participa eventualmente do complexo de podridões radicular sendo sua presença mais notória no final do ciclo deste complexo (CNPAF 2010).
O tombamento pode ocorrer durante a germinação ou estabelecimento da planta (fase de plântula), devido à incidência de fungos habitantes do solo ou associados às sementes. Em condições favoráveis, esses fungos causam necrose dos tecidos jovens e tenros do caule, cotilédones e raízes. O principal dano causado pelo tombamento é a redução do estande, sendo, muitas vezes, necessário o replantio, que elevam os custos de produção da cultura. A maioria dos fungos causadores de tombamento possui uma enorme gama de hospedeiros, principalmente R. solani e S. rolfsii. As culturas do algodoeiro, feijoeiro, cafeeiro, seringueira, morangueiro, tomateiro, alface, arroz, cebola, amendoim, batata, cana-de-açúcar, ervilha, fumo, pinus, soja, pimentão, tomateiro, citrus e mandioca são afetadas por esses patógenos (Suassuna e Coutinho, 2006).
O objetivo deste trabalho foi identificar descrever e apontar medidas de controle de S. rolfsii incidente no colo de feijoeiro.
As amostras de feijoeiro apresentando sintomas foram coletadas no dia 26 de fevereiro de 2010 na área experimental do Instituto Federal Goiano campus Urutaí, foram levadas para o Laboratório de Microbiologia, para processamento e submissão de câmara úmida.
Os materiais em câmara úmida foram depositados em caixas tipo Gerbox contendo ao fundo papel mata-borrão umedecido. Esta amostra permanecera, por um período de sete dias, sob condições ambientais (+ 25ºC), para exteriorização do crescimento micelial e verificação das estruturas fungicas. Observando-se que houve crescimento micelial do fungo, logo após foram preparadas lâminas semi-permanentes, não verificando-se esporulação. Para a coleta, foi utilizada uma piça e uma seringa, onde foi aplicado o método de “pescagem direta” retirando fragmentos do fungo e repicando sobre uma lâmina contendo gotas de fixador lactofenol cotton blue, afim de corar estruturas células vivas. Posteriormente foi depositada uma lamínula sobre a estrutura fúngica vedando com esmalte incolor para conservação do material. Observando-se o desenvolvimento do fungo em microscópio estereoscópico, os sintomas no hospedeiro foram retirados algumas microfotografias para registro e descrição dos sintomas e sinais.
Hospedeiro: Feijoeiro (Phaseolus vulgaris L.)
Família botânica: Fabaceae
Doença: Podridão-radicular-do-feijoeiro
Agente causal: Sclerotium rolfsii Sacc., cuja fase teleomórfica corresponde ao basidiomiceto Athelia rolfsii, mas este é raramente observado.
Local da coleta: Instituto Federal Goiano – campus Urutaí - GO
Data da coleta: 26/02/2010
Taxonomia: pertence ao reino Fungi, divisão Basidiomicota, classe Basidiomiceto, ordem Agaricales, família Typhulaceae, gênero Sclerotium sp. e espécie Sclerotium rolfsii (Índex Fungorum, 2010).
Sintomatologia
As lesões aparecem no colo ao nível do solo na forma de manchas escuras, encharcadas. Estendem-se pela raiz principal, produzindo uma podridão cortical recoberta por um micélio branco e numerosos esclerócios, inicialmente brancos e, posteriormente, marrom-escuros. Na parte aérea apresenta amarelecimento, desfolhação dos ramos superiores e uma murcha que conduz à seca total. Nas vagens próximas do solo o micelio ocasiona a podridão (Alves e Del Ponte, 2010).
Etiologia
O fungo Sclerotium rolfsii é habitante do solo e produz esclerócios, que são a principal forma de sobrevivência. Esta estrutura de resistência faz com que possa ter uma longevidade de mais de cinco anos no solo, em ambiente seco. Tanto os escleródios quanto o micélio são fonte de inoculo, pois o fungo pode sobreviver saprofiticamente em restos culturais na forma de micélio, que posteriormente formam os escleródios. (Agrofit, 2010).
O fungo S. rolfsii é uma sinonímia de Athelia rolfsii, onde a Atlhelia rolfsii tem como suas sinonímias o Botryobasidium rolfsii (Curzi) Venkatar, Corticium centrifugum (Lév.) Bres., Corticium rolfsii Curzi, Fibulorhizoctonia centrifuga (Lév.) G.C., Hypochnus centrifugus (Weinm.) Lév., Pellicularia rolfsii (Curzi), Rhizoctonia centrifuga Lév., Sclerotium rolfsii Sacc., (Species Fungorum, 2010).
A dispersão dá-se por meio de água da chuva e de irrigação, pelo solo aderido a máquinas e implementos agrícolas e por sementes contaminadas. Temperaturas elevadas entre 25 e 30 °C, umidade relativa maior que 90% e pH do solo abaixo de 6.0 são condições favoráveis à ocorrência da doença (Agrofit, 2010).
Epidemiologia
Segundo Alves e Del Ponte (2010), a disseminação do patógeno de um campo para outro se verifica principalmente pelo transporte de materiais infestados (solo, esterco, mudas e sementes), pelo homem, animais, vento, água e tratos culturais. O micélio pode passar pelo solo de uma planta para outra. A murcha só se desenvolve bem em condições de alta umidade, temperaturas entre 25-35 ºC e solos com boa aeração. Ferimentos na planta também favorecem a doença. O fungo S. rolfsii sobrevive de um ano para outro no solo na forma de esclerócio (estrutura de resistência) e de micélio.
Controle
Algumas práticas de manejo são recomendadas como não adubar a área de cultivo com esterco de animais que se alimentam de plantas doentes, pois os esclerócios não perdem a viabilidade no trato digestivo dos animais, efetuarem a drenagem adequada do solo, destruir pelo fogo as plantas doentes, realizar a rotação de cultura com milho, algodão, arroz e forrageiras, por no mínimo três anos, eliminar os restos de cultura, não acumular matéria orgânica junto ao colo da planta (Alves e Del Ponte, 2010).
Algumas medidas podem ser tomadas para reduzir os danos causados pela doença, como por exemplo, a rotação de cultura com cereais para reduzir o potencial de inoculo. Devem-se eliminar plantas daninhas suscetíveis ao patógeno e destruir e incorporar os restos de cultura. O plantio deve ser feito em solos com boa drenagem, evitando-se plantios densos e em solos ácidos. A redução da severidade da doença em solos pobres e ácidos tem sido obtida através de adubação equilibrada e calagem do solo, além do uso de variedades com certo nível de resistência como Rio Tibagi e IPA-10. A solarização pode ser uma medida eficiente para redução do número de escleródios viáveis no solo (Bianchini et al., 2005).
No mercado dois produtos químicos são registrados para controle de S. rolfsii no feijoeiro, cujo, nome dos produtos fitossanitários é: Cercobin 700 WP®, ingrediente ativo é o tiofanato-metílico (benzimidazol), são recomendados para aplicações terrestres, onde se empregam quantidades de água de 700 - 1000 litros/hectare ou assegurando a dose de 0,7 kg/ha., a primeira aplicação deverá ser realizada aos 20 dias após a emergência e as demais em pré e pós florada, realizar 3 aplicações e o Metiltiofan®, ingrediente ativo é o tiofanato-metílico (benzimidazol), são recomendados para aplicações terrestres, onde se empregam quantidades de água de 700 - 1000L/ha ou assegurando a dose de 0,7 kg/ha, no caso do feijão realizar 3 aplicações, a primeira aplicação deverá ser realizada aos 20 dias após a emergência e as demais em pré e pós florada (Agrofit, 2010).
O tratamento de sementes, com objetivo de controlar seus patógeno e dar proteção contra os do solo, é considerado como um dos métodos de baixo custo; representa de 0,1 % a 0,5 % do custo total da produção; é aplicado de forma localizada e em pouco volume. É de fácil aplicação, além de ser pouco poluente; causa menor impacto ao ambiente, se comparado com pulverizações da parte aérea. O tratamento de sementes traz como benefícios a manutenção ou melhoria da qualidade sanitária da semente, evita a disseminação ou introdução de patógeno, como fonte de inoculo primário e pode proporcionar bom estande inicial da cultura do feijoeiro (ITO, 2010).
Segundo ITO (2010), alguns produtos químicos podem ser utilizado para o tratamento de sementes como é o caso do KOTUBOL 750® que tem como princípio ativo quintozeno, sendo sua dosagem de 350 g/100 kg de semente de feijão e TERRACLOR 750 PM BR UNIROYAL® que também tem o quintozeno como princípio ativo e sendo sua dosagem de 150 a 300 g/100 kg de semente de feijão.
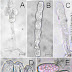
FIGURA 1 – Podridão-radicular-de-sclerócio (Sclerotium rolfsii Sacc.) no feijoeiro (Phaseolus vulgaris L.), A. sintoma de murcha da parte aérea, seca, queda das folhas e morte, B. crescimento micelial branco produzindo escleródios em condições de câmara úmida, C. escleródios imaturos (bar = 0,4mm), D. escleródios escuros de superfície lisa (bar = 1,3mm).
AGROFIT. Disponível em:
ALVES, R.C., DEL PONTE, E.M. Requeima da batata. In: Del Ponte, E.M. (Ed.) Fitopatologia.net - herbário virtual. Departamento de Fitossanidade. Agronomia, UFRGS. Disponível em: <http://www.ufrgs.br/agronomia/fitossan/herbariovirtual /ficha.php?id=101>. Acessado em: 29 de junho de 2010.
BIANCHINI, A.; MARINGONI, A. C. e CARNEIRO, S.M.T.P.G.; Doenças do feijoeiro (Phaseolus vulgaris). KIMATI, H.; AMORIM, L.; REZENDE, J.A.M.; BERGAMIN FILHO, A.; CAMARGO, L.E.A.; Manual de fitopatologia: Doenças das plantas cultivadas. 4ª Ed. Vol. 2, pag. 344-345 – São Paulo: Agronômica Ceres, 2005.
CARDOSO, J.E. Podridão do colo. In: Sartorato, A. & Rava, C.A. (Eds.). Principais doenças do feijoeiro comum e seu controle. Brasília: Embrapa -Arroz e Feijão. 1994. p. 165-173.
CNPAF. Disponível em: <http://www.cnpaf.embrapa.br/feijao/pragasedoencas/ podridaodocolo.htm> acessado em: 28 de março de 2010.
FARR, D.F., & ROSSMAN, A.Y. Fungal Databases, Systematic Mycology and Microbiology Laboratory, ARS, USDA. Disponível em: <http://nt.ars-grin.gov/fungaldatabases/> acessado em: 25/06/10.
INDEX FUNGORUM. Disponível em: <http://www.indexfungorum.org/names /Names.asp> acessado em: 23 de junho de 2010.
ITO, M.F.; et al. INFORMAÇÕES TÉCNICAS: Importância do uso de sementes sadias de feijão e tratamento químico, 14 p., Disponível em: <> acessado em: 29 de junho de 2010.
MENDES, M. A. S.; URBEN, A. F.; Fungos relatados em plantas no Brasil, Laboratório de Quarentena Vegetal. Brasília, DF: Embrapa Recursos Genéticos e Biotecnologia. Disponível em:
PUNJA, Z.K. The biology, ecology and control of Sclerotium rolfsii. Annual Review of Phytopathology, 23:97-127. 1985.
SPECIES FUNGORUM. Disponível em: <http://www.speciesfungorum.org/Names /SynSpecies.asp?RecordID=309351> acessado em: 30 de junho de 2010.
SUASSUNA, N.D.; COUTINHO, W.M. MANEJO DAS PRINCIPAIS DOENÇAS DA MAMONEIRA. In: Tropical Brazilian Phytopathological. 31 (suplemento), 76 p., agosto 2006.