FERRUGEM DO JAMBO AMARELO (Syzygium jambos) CAUSADO POR Puccinia psidii
Gabriel Pereira de Souza
Acadêmico do curso de
Agronomia
INTRODUÇÃO
O
jambo-amarelo Syzygium jambos (L.) Auston (sinonímia: Eugenia jambos L.)
(Myrtaceae), conhecido vulgarmente como “jambo amarelo, jambo-comum,
jambo-da-índia, jambo-cheiroso ou jambo-verdadeiro”, é uma espécie arbórea
originária da Ásia Tropical (Leste da Índia e Malásia). Não foram encontrados
registros sobre a época de introdução do Syzygium jambos na Mata
Atlântica brasileira. No entanto, é bastante sensato acreditar que a as primeiras
introduções tenham ocorrido entre os séculos XVIII e início do século XIX
(CARVALHO, 2005).
O jambeiro é uma espécie de
arvore sempre-verde, tolerante a sombra, que se estabelece melhor em condições
de forte sombreamento, onde ocupa o estrato médio da floresta. Possui grande
plasticidade à condições ambientais adversas, e fácil adaptação à ambientes de
florestas tropicais úmidas. Apresenta diferentes utilidades ao uso humano. Seus
indivíduos são usados como quebra ventos e para controle de erosão. Sua madeira
é amplamente usada como combustível e para extração de tanino. Embora apresente
baixa qualidade, sua madeira também é usada na construção civil e confecção de
artesanatos. Seus frutos são bastante apreciados para consumo humano e usados
para produção de doces e geleias. Em algumas regiões, madeira, raízes, frutos e
sementes costumam ser utilizados na medicina popular. Existe o interesse no cultivo da espécie, que
pode ser observada como árvore ornamental em diversas cidades e áreas rurais (CARVALHO.
2005)
O
fungo Puccinia psidii ataca indistintamente todos os tecidos novos das plantas em
desenvolvimento. Em plantas adultas, inicialmente aparecem pequenas pontuações
amareladas e necróticas, que evoluem para manchas circulares, necróticas, de
coloração amarela, recobertas por uma densa e pulverulenta massa, de coloração
amarela - viva, formada pelos uredósporos e teliósporos do fungo. Com o tempo,
essa massa amarela desaparece, permanecendo somente a área necrótica e seca,
frequentemente apresentando rachaduras. Sendo assim, de grande importância,
podendo causar em ataques intensos, perdas na ordem de 80 a 100% dos frutos.
Estes quando atacados desde as primeiras fases de desenvolvimento, caem em
grande quantidade ou permanecem na planta e mumificam-se (KIMATI et al.,
1997).
A ferrugem
é uma das principais doenças da família Mirtaceae, sendo causada pelo
fungo P. psidii, e sabe-se hoje que todos os membros dessa
família botânica são hospedeiros para a doença. Portanto, ficou conhecida como
“Ferrugem das Mirtáceas”. Trata-se de uma ferrugem neotrópica, nativa da
América do Sul e encontra-se amplamente distribuído nas Américas do Sul e Central
e nas ilhas do Caribe (FOURNIER et al., 1998), com um imenso
número de hospedeiros nativos, silvestres ou cultivados. Mas, a capacidade notável
de P. psidii de se adaptar e infectar mirtáceas importadas e
não originárias da América do Sul, caso do jambeiro e do eucalipto, traz um
problema ainda maior para o cultivo dessas espécies (FIGUEREIDO, 2001) .
Objetivos
O
objetivo deste boletim técnico é descrever a sintomatologia, etiologia,
epidemiologia e controle de ferrugem do jambo amarelo causado por Puccinia psidii.
DESENVOLVIMENTO
Hospedeiro/cultura: Jambo-amarelo
(Syzygium jambos (L.) Alston)
Família Botânica: Myrtaceae
Doença: Ferrugem
Agente
Causal: Puccinia psidii G. Winter
Local de
Coleta: Urutai /GO
Data de
Coleta: 25/02/2015
Sinonímias: Bullaria
psidii (G. Winter) Arthur & Mains (1922) e, também, Dicaeoma
psidii (G. Winter) Kuntze (1898) (INDEX FUNGORUM, 2015).
Taxonomia: O fungo
pertence ao reino Fungi, divisão Basiodiomycota, classe Pucciniomycetes, ordem
Pucciniales, família Pucciniaceae, gênero Puccinia psidii G. Winter
(INDEX FUNGORUM, 2015).
Sintomatologia: O patógeno infecta tecidos
jovens como folíolos, inflorescências, gemas e frutos novos (SILVEIRA, 1951;
GALLI, 1980; SOUZA, 1985; FERREIRA, 1989).
Nas folhas os sintomas têm início
com pequenas manchas amareladas (Fig. 1G), geralmente circulares elípticas,
recoberta pela cutícula da planta. Com o desenvolvimento da doença estas
manchas aumenta de tamanho se rompe a massa de urediniósporos produzida pelo
patógeno. Neste estádio as manchas são denominadas pústulas e apresentam
coloração amarelas ou alaranjadas (Fig.1C). Quando mais velhas, as manchas
tornam se castanhas ou pretas em decorrências do surgimento dos teliósporos
sucedâneos dos urediniósporos. As
pústulas apresentam salientes em relação a superfície foliar e podem coalescer
quando a doença ocorrem com alta intensidade (SANTOS & MENDES, 2015).
Portanto Santos & Mendes (2015),
afirma que com o passar do tempo, essa massa amarela desaparece, permanecendo
apenas uma área necrótica seca e frequentemente apresentando rachaduras (Fig. 1F.).
É quando em condições ambientais favoráveis à doença, as lesões se coalescem,
ocasionando a morte do limbo, resultando em grande perda de tecidos e queda das
folhas.
Segundo
JUNQUEIRA et al. (2001) nas flores e nos botões florais quando são
atacados pela ferrugem na fase inicial do seu desenvolvimento, exibem lesões
circulares, de diâmetros variáveis e são recobertas por uma massa pulverulenta
de coloração amarela intensa que podem causar a perda parcial ou total da
produção. Nos ramos e frutos a ferrugem produz manchas recoberta por uma densa
massa pulverulenta amarela, constituída por urediniósporos do patógeno quando
ocorrem a coalescência destas lesões, os ramos novos e os frutos jovens podem
ficar totalmente recobertos por essa massa (Fig.1D). As manchas com o decorrer
do tempo podem se torna necróticas (BERGAMIM FILHO et al., 2011). Os frutos que forem atacados
e que permanecerem na planta mumificam-se, tornando-se deformados e sem valor
comercial, servindo como uma porta de entrada para vários microrganismos secundários
responsáveis por podridões (JUNQUEIRA et al., 2001).
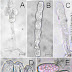
Figura
1. Ferrugem das mirtáceas causada por
Puccinia psidii nas folhas de jambo
amarelo. A. Plantas com sintomas em brotos jovens (bar: 2mm). B. Detalhe
do broto jovem com abundante pulverulência (bar: 3 mm). C. Ramo com
superfície apresentando abundante pulverulência de coloração alaranjada (bar:1 mm).
D. Pecíolos da sépala em fruto de jambo com presença de (bar: 4 mm). E.
Detalhe da lesão, mancha foliar necrótica com halo clorotico avançado na
face abacial (bar: 5 mm). F. Face adaxial mostrando com detalhe mancha
esférica e necrótica com halo amarelo e clorotico (bar: 4mm). G. Sintoma
de lesão pulverulenta na face adaxial em estagio de formação abundante de
urediniosporos (bar: 6 mm). H. Face abaxial apresentando pulverulência
(bar: 6 mm).
Etiologia: O fungo causador da doença, P.
psidii, um basidiomiceto pertencente à ordem Uredinales, é um parasita
obrigatório e apresenta alta especificidade em relação ao hospedeiro. A
colonização dos tecidos vegetais é feita através do crescimento micelial
intercelular e da emissão de haustórios intracelulares (KIMATI et al.,
1995)
O fungo P.
psidii é um patógeno de ciclo curto, da qual
se conhecem seus estádios I – écio (FIGUEIREDO et al., 1984), II – urédia, III
– télia e IV – basídio (MACLACHLAN, 1938; FERREIRA, 1983). Até então o estádio
espermogonial é desconhecido, mas é provável que não exista. O estádio I – écio
apresenta a mesma morfologia do estádio II – urédia e teve sua ocorrência
mostrada, até o momento, apenas no jambeiro (FIGUEIREDO et al., 1984), mas
provavelmente também ocorra nas demais mirtáceas hospedeiras do patógeno. O
estádio II é constantemente produzido em condições naturais ou em inoculações
artificiais e, inclusive, é por meio de suas pústulas uredospóricas, de
coloração amarela que, em termos práticos, se faz o diagnóstico da doença em
condições de campo. Individualmente, uma pústula bem desenvolvida pode ter mais
de 20 urédias, cada uma com 0,2 – 0,3 mm de diâmetro. As pústulas podem
interligar-se, e isso acontece, especialmente quando os primórdios foliares e
as partes apicais tenras dos galhos e da haste principal se mostram totalmente
cobertos pela esporulação. Esta esporulação aparece tomando ambas as faces dos
primórdios foliares, mas, nas folhas um pouco mais desenvolvidas, é muito mais abundante
nas faces inferiores dos limbos. Os urediniósporos variam quanto à forma,
predominando os piriformes e de esféricos a ovais, que apresentam leves
esquinulações na parede externa e medem 10-20 x 15-25 μm (Tab. 1).
Dessa
forma, necessita de hospedeiro vivo para seu desenvolvimento e, em função da
sua especialização em relação ao hospedeiro, geralmente não possui hospedeiro
alternativo. Portanto nos trópicos, o patógeno sobrevive principalmente na
forma de urediniósporos que, geralmente, permanecem sobre plantas voluntárias
após a colheita. Mas em muitas situações, os teliósporos atuam como estruturas
de resistência e garantem a sobrevivência do patógeno na ausência do hospedeiro
(KIMATI et al., 1995).
Em plantas de jambeiro os teliósporos têm sido
facilmente encontrados, na época mais quente do ano, de dezembro a março,
sendo, inclusive, as pústulas constituídas de mistura de teliósporos e
urediniósporos, reconhecidas a olho nu por suas tonalidades mais castanhas, em
contraste com as pústulas amarelo-vivas, que contêm apenas urediniósporos. Os
teliósporos de P. psidii são pedicelados, bicelulares, clavados,
achatadamente, muitos com uma papila apical na parede da célula posterior e
medem 15-28 x 30-60 μ m (FERREIRA, 1989).
Figura 2. Sinais de Puccinia psidii oriundo de folhas de jambo amarelo A. Corte histológico
mostrando a interação do fungo com a parede celular do vegetal na fase da urédia
(bar: 145 μm). B. Urediniósporo (bar: 25 μm). C. Urediniósporos
(bar: 15 μm). D. Teliósporos com papila visível (bar: 37 μm). E. Teliósporos
com pedicelo visível (bar: 10 μm). F. Teliósporo sem papila (bar:27 μm).
G. Teliósporo com pedicelo desenvolvido (bar: 42 μm). H Teliósporos
bicelulares e clavados (bar:19,7 μm). I. Urediniósporos esféricos
e clavados (bar: 15 μm). J. Teliósporos e Urediniósporos (bar: 9 μm).
Tabela 1. Aspectos morfológicos e morfométricos de Puccinia psidii identificado em jambo-amarelo comparado com dados morfológicos descritos por Kimati et al. (1997).
|
Características
morfológicas
|
Isolado
|
KIMATI
et al. (1997)
|
|
Dimensão da
lesão
|
4-(3)-2
mm
|
5
mm
|
|
Dimensão do
Urediniósporos
|
17,07
- ( 19,26 ) - 11,42 X 25,14 - (14,71 ) -16,49 μ m
|
10
x 20 a 15 x 25 μ m
|
|
Forma do
Urediniósporos
|
Esférica,
elíptica e clavada
|
Piriformes,
esféricas ou ovais
|
|
Dimensão do Teliósporos
|
21,45
- (17,59) - 13,68 X 42,4 - (34,82 ) - 24,83 μ m
|
15-28 x 30-60 μ m
|
|
Dimensão do
pedicelo
|
|
Nd
|
|
Forma do Teliósporos
|
Clavado
|
Clavado
|
|
Número de
células do teliósporos
|
Bicelular
|
Bicelular
|
Epidemiologia: O fungo P. psidii apresentou 725 registros de
ocorrência infectando os seguintes hospedeiros: infectando Abbevillea maschalantha no Brasil (HENNEN, et al. 1982.), Acmena hemilampra, Acmena smithii, Anetholea
anisata ,Asteromyrtus
brassii, Austromyrtus dulcis, Austromyrtus
sp., Austromyrtus tenuifolia, Backhousia angustifolia, Backhousia bancroftii, Backhousia citriodora, Backhousia hughesii, Backhousia leptopetala, Backhousia myrtifolia, Backhousia oligantha , Backhousia sciadophora na Australia
(PEGG, et al. 2013), Acmenosperma claviflorum na Australia (PEGG, et al. 2014), Agonis flexuosa na Australia ( ROUX et al.
2013), Callistemon speciosus, Campomanesia adamantium, C.
aurea, C. maschalantha e C. moschalantha no Brasil (MENDES, et al. 1998.), Calycorectes riedelianus no Paraguai (LINDQUIST. 1982), Chamelaucium uncinatum, Corymbia citriodora subsp. variegata, Corymbia
henryi, Corymbia torelliana, Darwinia citriodora, Decaspermum
humile na Austrália (GIBLIN. 2013), Eucalyptus camaldulensis em Taiwan (PEGG, et al. 2013), E. capitata, E. citriodora, E. grandiflora, E. phoenicea, Eugenia stipitata, E.
uvalha, no Brasil (PEGG, et al. 2013), Eucalyptus
carnea, E. cloeziana, E. curtisii, E. grandis, E. phaeotricha, E. planchoniana, Eucalyptus sp., E. tereticornis, E. tindaliae na Austrália (GIBLIN,
2013), E. globulus, Eugenia brachythrix na Jamaica (DALE, 1955),
E. brasiliensis, E. cambucae, E. dysenterica, E. grandis, E. malaccensis no Brasil (HENNEN, et al.
1982.), Eugenia caryophyllata, E. glaucescens, E. jambos na Argentina, Brasil, Colômbia, Cuba, República
Dominicana, Jamaica, Paraguai e Porto Rico (LINDQUIST, 1982.), Eugenia
natalitia na Austrália, Eugenia
pungens na Argentina, Brasil
e Uruguai (GIBLIN, 2013),
Eugenia reinwardtiana na
Australia, Eugenia
sp. Argentina, Brasil, Costa Rica, Jamaica (HENNEN et al. 1982.),
Eugenia uniflora no Australia e Brasil, Eugenia
zeyheri, Gossia
acmenoides, G.
bamagensis, G. bidwillii, G. floribunda, G. fragrantissima, G. gonoclada, G. hillii, G. inophloia, G. lewisensis, G. macilwraithensis, G. myrsinocarpa, G. punctata
na Austrália (GIBLIN, 2013 ), Heteropyxis natalensis na África (ALFENAS, 2005), Homoranthus melanostictus, H. papillatus, H. virgatus, Hypocalymma angustifolium, Heteropyxis natalensis
na África, Homoranthus melanostictus, H. papillatus, H. virgatus, Hypocalymma angustifolium na Austrália (HENNEN, et al. 1982. ), Jambosa jambos no Brasil,
Colômbia, Cuba, Paraguai e Porto Rico (HENNEN et al. 1982.), Jambosa
vulgaris em Cuba, Lenwebbia lasioclada, L. prominens, Lenwebbia sp., Leptospermum liversidgei, L. luehmannii, L. madidum, L. petersonii, L. semibaccatum, L. trinervium, Lindsayomyrtus racemoides, Lophostemon suaveolens, Melaleuca fluviatilis, M.
formosa, M. leucadendra, M. leucadendron, M. linariifolia, M. nervosa, M. nesophila, M. nodosa, M. pachyphylla, M. paludicola, M. polandii, M. salicina, M. saligna, M. viminalis, M. viridiflora, Metrosideros collina , M. kermadecensis, Mitrantia bilocularis na Austrália, Metrosideros polymorpha no
Hawai e Japão, Myrcia
caracasana na Venezuela, Myrcia
jaboticaba no Brasil (CHARDON et al., 1930), Myrcia
sp. no Brasil, Myrcia
stenocarpa, Myrcia
xylopioides na Colômbia, Myrcianthes pungens no Uruguai, Austrália e Brasil, Myrciaria jaboticaba, Myrciaria plicato-costata, Myrtaceae no Brasil e Colômbia
(CHARDON et
al. ,1930), Phyllocalyx involucratus no Brasil, Pilidiostigma glabrum, Pilidiostigma tetramerum, Pimenta
acris na Jamaica, Pimenta dioica no Brasil, EUA, Jamaica, Mexico, Pseudomyrcianthes
pomifera, Pseudomyrcianthes pyriforme, Psidium
araca, Psidium
guineense, Psidium incanescens, Psidium sp. no Brasil, Rhodamnia angustifolia, R.
arenaria, R. argentea, R. blairiana, R. costata, R. dumicola, R. glabrescens, R. maideniana, R. pauciovulata, R. rubescens, R. sessiliflora, R. spongiosa, Rhodomyrtus tomentosa, Rhodomyrtus trineura subsp. capensis, Ristantia waterhousei, Sphaerantia discolor, Stockwellia quadrifida, Syzygium angophoroides, S. apodophyllum, S. aqueum, S. argyropedicum, S. armstrongii, S. australe, S. bamagense, S. banksii, S. boonjee, S. canicortex na Austrália. Syzygium jambos na Austrália, Brasil, China,
Colômbia, Costa Rica, EUA, Havai e Uruguai,
Tristania neriifolia, Tristaniopsis exiliflora, T. laurina, Uromyrtus tenella, Waterhousea floribunda, W. hedraiophylla, W. mulgraveana, W. unipunctata, Xanthostemon chrysanthus, X. oppositifolius, X. youngii na Austrália (GIBLIN, 2013; FARR & ROSSMAN, 2015).
No mundo tem sido registrado este patógeno em
vários gêneros e 154 espécies de plantas hospedeiras representadas por Myrtales nas famílias Heteropyxidaceae
sobre o gênero Heteropyxis e
Myrtaceae sobre os gêneros Abbevillea
sp., Callistemon sp., Calycorectes sp., Campomanesia sp., Eucalyptus
sp., Eugenia sp., jambosa sp., Marlierea sp., Melaleuca
sp., Myrcia sp., Myrciaria sp., Phyllocalyx
sp., Pseudomyrcianthes sp., Psidiopsis sp., Psidium
sp., Siphoneugena sp. e Syzygium sp. (FARR, & ROSSMAN,
2015).
Este
fungo infecta vários gêneros e um
númeras espécies nas Myrtales, que
inclui culturas arbóreas de importância econômica tais como Eucalyptus spp, officinalis
pimento (pimenta da Jamaica), Psidium
guajava (goiabeira) e Syzygium
aromaticum (cravo). A espécie P. psidii é endémica das Américas. Embora Eucalyptus originado na Austrália e na
região do Sudeste da Ásia são suscetíveis a P.
psidii. A ferrugem pode produzir danos significativos em mudas e árvores
jovens no Mundo e é uma ameaça potencial
para a os vários milhões de hectares de plantações de eucalipto em todo o
mundo. Devido a isto, muito controle e
realizdo para que a ferrugem não se
espalhe para novas áreas (COUTINHO, et al. 1998). A goiabeira - P. psidii causa uma doença grave em goiaba infectando folhas, caules e frutos, causando desfolha e
mumificar frutos quando a infecção ocorre no início. Esta ferrugem também ataca
folhagem, inflorescências, e jovens suculentos frutos, eucalipto e Syzygium (FARR, &
ROSSMAN,2015).
Para
BLUM e DIANES (2001), a formação de orvalho é um dos fatores determinantes de
novas infecções e produção de novos urediniósporos de P. psidii. Além da
formação de orvalho, outras condições ambientais favoráveis como temperaturas
menores que 20 °C, umidade relativa alta, em torno de 80%, e longo período de
molhamento são necessárias à germinação, penetração e infecção do fungo, além
de favorecer também elevados índices de produção de esporos e aumento da doença.
Já temperaturas muito elevadas são adversas ao patógeno e, caso a infecção já
tenha ocorrido, induzem à formação de teliósporos (estruturas de resistência),
além de ocorrer necrose de parte do tecido foliar e, posteriormente,
senescência da folha infectada (APARECIDO, 2009).
Portanto, a disseminação pode ocorrer a curtas ou a longas distâncias através
do vento, da água, insetos e outros agentes disseminadores. A água, na forma de
respingos, tem papel importante na disseminação dos esporos dentro da planta ou
para plantas vizinhas. O vento, no entanto, é o agente de maior importância.
Além de promover a disseminação dentro da planta e para plantas próximas, dessa
forma, promove uma distribuição eficiente do inóculo em amplas áreas
geográficas (KIMATI et al., 1995).
As espécies deste patógeno tem ocorrência
neste seguinte países: Austrália,
América do Sul, América Central e Caribe, América do Norte, México, EUA, África
(África do Sul). Relatórios da Ásia (Taiwan, Índia) não são confiáveis
(INDEX FUNGORUM, 2015). Além do jambo-amarelo, o mesmo fungo foi identificado
em mais outras 153 hospedeiras, como por exemplo em goiaba, Psidium guajava,
na Argentina, no Brasil e na Colômbia, espécies de Eucalipto, como Eucalyptus
captata registrado no Brasil, no Uruguai entre outras (FARR & ROSMAN,
2011)
CONTROLE
Controle
cultural: Portanto utiliza as praticas culturais como: Promover um melhor
arejamento e insolação do pomar através de podas e desfolhas. Realizar a poda
em períodos com condição climática desfavorável à ocorrência da doença.
Erradicar das proximidades do pomar variedades muito susceptíveis e/ou
Mirtáceas que possam servir de fonte de inoculo permanente, e, se possível
instalar o pomar em locais que apresentem baixa umidade relativa ou menor período
chuvoso. . Realizar adubação adequada, de acordo com a análise do solo,
evitando excesso de adubação nitrogenada (AGROFIT, 2015).
Controle
químico: utiliza pulverizações preventivas com fungicidas cúpricos que
podem ser realizadas em frutos com até 3 cm de diâmetro. Após este tamanho, os
frutos são sensíveis ao cobre. Quando as pulverizações preventivas não
controlarem a doença, realizar pulverizações curativas com o uso de produtos à
base de oxicloreto de cobre, hidróxido de cobre, óxido cuproso e calda
bordalesa (AGROFIT. 2015). Para a cultura do jambo amarelo não há registros de
ingredientes ativos, mas para controle de p.
psidii existe somente produtos registrados para a cultura da goiaba e estes
são representado por: ciproconazol (triazol)®, azoxistrobina
(estrobilurina) + difenoconazol (triazol)® ,
azoxistrobina (estrobilurina)®, oxicloreto de cobre®
(inorgânico), Óxido Cuproso®
(inorgânico) , bromuconazol®
(triazol) , tebuconazol®
(triazol) , tebuconazol (triazol) + trifloxistrobina®
(estrobilurina), Sulfato tribásico de Cobre® (inorgânico), sulfato de
cobre® (inorgânico) e azoxistrobina® (estrobilurina) (AGROFIT.
2015) .
Desde
a década de 1980, o triadimenol é o fungicida mais utilizado para o controle da
ferrugem. No mercado há vários fungicidas eficientes para o controle de
ferrugens, conforme a tabela acima, como as estrobilurinas e os triazóis. As
estrobilurinas têm atividade biológica variada e potencial de controle de ampla
gama de fungos. Inibem a respiração mitocondrial ao bloquearem a transferência
de elétrons entre os citocromos B e C, o que interfere na formação de ATP,
atuando nos estádios de pré-penetração e inibindo a germinação de esporos, o
desenvolvimento de tubos germinativos e a formação de apressórios. Apresentam,
também, ação curativa, por inibirem o desenvolvimento do fungo nos estágios
pós-germinação e causarem o colapso do micélio dentro do tecido colonizado, bem
como ação anti-esporulante (ZAUZA, et al., 2008).
Segundo ZAUZA, et al.,
2008, a maioria dos fungicidas do grupo dos triazóis Tem efeito fungitóxico
elevado, porque ocorre a penetração e translocação rápida nos tecidos vegetais,
o que evita perda por lixiviação, tornando o efeito residual prolongado, assim e
age como protetor nos eventos pré-penetração e como curativo nos eventos
pós-penetração, mas este tem ação sistêmica acropetal, inibindo a
biossíntese de esteróis, especialmente do ergosterol. A deficiência desse
esterol e o acúmulo de compostos intermediários induzem a formação de membranas
alternativas e a desorganização celular.
Controle
Genético: Para Kimati, et al. (1995) as forma mais viável de
controle e a utilização de variedades resistentes. Portanto, a resistência
genética é o melhor controle da ferrugem, sendo menos poluente e mais
econômico. Dessa forma, o melhoramento
genético para resistência durável é a alternativa de continua superação da
resistência das cultivares, devido a alterações na população patogênica, que
resultam em novas raças (BARCELLOS, 2007).
LITERATURA CITADA
AGROFIT, disponível em:
http://extranet.agricultura.gov.br/agrofit_cons/principal_agrofit_cons.
Acessado em: 06/05/2015.
ALFENAS, A.C., ZAUZA, E.A.V., WINGFELD, M.J.,
ROUX, J., E GLEN, M. 2005.
Heteropyxis natalensis, a new host
of Puccinia psidii rust. Australas. Pl. Pathol. 34:
285-286. (39912).
CHARDON, C.E., and Toro, R.A. 1930. Mycological explorations of Colombia. J.
Dept. Agric. Porto Rico 14: 195-369. (5035)
APARECIDO, C.C. Ecologia de Puccinia
psidii, agente causal da ferrugem das mirtáceas. 2009. Artigo em
Hypertexto. Disponível em: . Acesso em: 15/4/2015
BARCELLOS, A.L. Combate à
Ferrugem. Cultivar. Junho de 2007.
BLUM, L.E.B.;
DIANESE, J.C. Padrões de liberação de urediniósporos e desenvolvimento da
ferrugem do jambeiro. Pesquisa Agropecuária Brasileira. Brasília – DF. 2001.
Carvalho F.A.
SYZYGIUM JAMBOS (L.) AUSTON
– UMA INVASORA NA MATA ATLÂNTICA?. 2005.13f. Dissertação (Doutorado em
Ecologia) - Universidade de Brasília, Brasília, 2005.
COUTINHO, T.A., WINGFIELD, M.J., ALFENAS, A.C.,
and Crous, P.W. 1998.
Eucalyptus rust: a disease
with the potential for serious international implications. Pl. Dis. 82:
819-825.
GIBLIN,
F. 2013.
Myrtle rust report: New Caledonia. University of the Sunshine Coast : 1-18. (46706)
FOURNIER LA, DI STEFANO JF, CARRANZA J, MARIN
W, MORA A, 1998. potencial invasivo de Syzigium jambos (Myrtaceae) em fragmentos
florestais: o caso de Costa Rica. Revista
de Biologia Tropical, 46: 567-573.
Disponível
em : http://www.indexfungorum.org/names/Names.asp
. Acesso em: 12 de abrilde 2015.
Disponível em: http://nt.arsgrin.gov/fungaldatabases/fungushost/new_frameFungusHostReport.cfm. Acesso em 10 de abril de 2015.
FARR & ROSMAN, SBML Systematic
Botany of Mycological Resources. Disponível em:. Acesso em: 15 de abril
de 2015.
FIGUEIREDO, B.M. Palestra: Doenças Fúngicas emergentes
em Grandes Culturas. Centro de Pesquisa e Desenvolvimento de Sanidade Vegetal
do Instituto Biológico. São
Paulo – SP. 2001
Hernández, J.R. Systematic Mycology and
Microbiology Laboratory, ARS, USDA. 27 February 2006. Invasive Fungi. Puccinia psidii. Retrieved April 13,
2015, from /sbmlweb/fungi/index.cfm .
Hennen,
J.F., Hennen, M.M., and Figueiredo, M.B. 1982. [Index of the rust fungi (Uredinales) of
Brazil]. Arch. Inst. Biol. (Sao Paulo), Suppl. 1 49: 1-201. (5819)
INDEX FUNGORUM.
Disponível em: . Acesso em: 28 de março de 2015.
JUNQUEIRA, N.T.V.; ANDRADE, L.R.M.; PEREIRA, M.; LIMA,
M.M.; CHAVES, R.C. Doenças da Goiabeira no Cerrado. Circular Técnica nº15.
EMBRAPA CERRADOS. Planaltina-DF. 2001
KIMATI, H.; AMORIM, L.; BERGAMIN FILHO, A.; CAMARGO, L.E.A.; REZENDE,
J.A.M. Manual de Fitopatologia: doenças das plantas cultivadas. , Vol. II,
Editora Agronômica Ceres Ltda, São Paulo SP. 1997.
KIMATI, H.; AMORIM, L.; BERGAMIN
FILHO, A. Manual de Fitopatologia: princípios e conceitos. 4a Ed, Vol. I,
Editora Agronômica Ceres Ltda, São Paulo SP. 2011.
Kern,
F.D., Thurston Jr., H.W., and Whetzel, H.H. 1933. Annotated index of the rusts of
Colombia. Mycologia 25: 448-503. (5034)
LINDQUIST, J.C. 1982. Royas de
la Republica Argentina y Zonas Limitrofes. Inst. Nacional de Tecnologia
Agropecuaria., 574 pages. (11172)
MENDES, M.A.S., DA SILVA, V.L., DIANESE, J.C.,
and et al. 1998. Fungos em Plants no Brasil.
Embrapa-SPI/Embrapa-Cenargen, Brasilia, 555 pages. (34636)
Pardo-cardona, V.M. 1998.
Registros nuevos para la flora de Uredinales (royas) de Colombia. Rev. Acad. Colomb. Cienc. 22:
347-354. (36874)
PEREZ,
C.A., WINGFIELD, M.J., ALTIER, N.A., SIMETO, S., AND BLANCHETTE, R.A. 2011. Puccinia psidii
infecting cultivated Eucalyptus and native myrtaceae in Uruguay. Mycol.
Progr. 10: 273-282. (45120)
ROUX, J., GREYLING, I., COUTINHO,
T.A., VERLEUR, M., AND WINGFIELD, M.J. 2013. The Myrtle rust pathogen, Puccinia psidii,
discovered in Africa. IMA Fungus 4: 155-159. (46705)
SANTOS, C. E. N., MENDES, M. A. S.; 2015.
http://extranet.agricultura.gov.br/agrofit_cons/principal_agrofit_cons.
Acessado em: 06/05/2015
ZAUZA, E.A.V; COUTO, M.M.F.;
MAFFIA, L.A.; ALFENAS, A.C. Eficiência de Fungicidas Sistêmicos no Controle da
Ferrugem do Eucalyptus Departamento de Fitopatologia da Universidade
Federal de Viçosa (UFV), 2008.




Vocês não vão acreditar no que eu li agora mesmo.
ResponderExcluirCara, eu fiquei abiasmado com o que acabei de encontar.
Eu estava pesquisando sobre jambo e consta uma informação no texto que me deixou curioso, consta lá que as sementes do jambo amarelo são muito venenosas.
Cara, que negócio doido, ainda bem que não mordi as sementes.
Chega me arrepiar em pensar que eu poderia, por curiosidade, lascar o dente naquela semente.
A informação mais relevante é que uma quantidade desconhecida de ácido cianídrico foi encontrada nas raízes, caules e folhas. Além disso, um alcalóide, a jambosina, foi encontrado na casca da árvore e nas raízes, e as raízes são consideradas venenosas.
Alguém sabe me informar se essa informação procede? Se alguém puder me ajudar com isso, ficarei muito grato.
Se eu encontrar algo primeiro, volto aqui para avisar se a informação é procedente.