Maurílio de Sousa Netto
Acadêmico do curso de Agronomia
1. INTRODUÇÃO
O cinamomo ou árvore-de-santa-bárbara (Melia azedarach - Meliaceae) é uma planta nativa do Sul da Ásia. Possui azadiractina, substância com propriedade inseticida, muito usada no controle alternativo de pragas (BRUNHEROTTO & VENDRAMIM, 2001).
Conhecida popularmente como árvore de Santa Bárbara ou cinamomo, a M. azedarach L. é uma espécie arbórea de até 20 metros de altura que produz uma madeira de cor esbranquiçada a avermelhada, com veios castanhos. O cinamomo é uma planta nativa do Sul da Ásia, atualmente, é muito utilizada para arborização urbana, pois apresenta flores aromáticas e tem folhagem caduca. Popularmente, é uma planta que apresenta uso inseticida, sendo que o extrato de suas folhas é utilizado na forma de pulverização sobre insetos pragas (BRUNHEROTTO & VENDRAMIM, 2001).
No Brasil as principais doenças que afetam o cinamomo são representadas pelo oídio (Oidium sp.), verrugose (Sphaceloma mileae) e a cercosporiose (Cercospora meliae).
Os fungos cercosporiódes estão freqüentemente associados às manchas foliares, bem como a flores, frutos e sementes de cereais, hortaliças, de plantas ornamentais, de essências florestais e de gramíneas. Apresentam ampla dispersão geográfica, podendo ser encontrados desde as zonas temperadas até os trópicos. Agrupados inicialmente no complexo gênero Cercospora Fresen, esses fungos foram recentemente desmembrados em gêneros menores, utilizando-se, inclusive, estudos de biologia molecular. Muito embora alguns aspectos tenham sido resolvidos, alguns gêneros afins ainda apresentam posição duvidosa (BRAUN et al., 2003).
Existem registrados no mundo infectando cinamomo os seguintes táxons de fungos cercosporóides: Cercoseptoria dominguensis, Cercospora appii, C. congoensis, Passalora congoensis, C. leucosticta, C. meliae, C. meliicola, C. subsessilis, Pseudocercospora subsessilis e Pseudocercospora meliicola (FARR & ROSSMAN, 2011).
Os conídios do isolado em questão mais se aproximam de C. congoensis e C. subsessilis, e como o primeiro apresenta conídios mais largos, identificou-se o agente causal da cercosporiose-do-cinamomo como sendo Pseudocercospora subsessilis Syd. & P. Syd. (SOUSA NETTO et al., 2011a; SOUSA NETTO et al., 2011b) (Tab. 1).
As suas sinonímias são: Cercospora subsessilis Syd. & P. Syd., Annals mycol. 11(3): 329 (1913); Cercosporina subsessilis Syd. & P. Syd. Sacc., Syll. fung. (Abellini) 25: 911; Cercoseptoria domingensis Cif. 1938; Pseudocercosporella indica A.N. Rai, B. Rai & Kamal 1993; Pseudocercospora meliae A.N. Rai & Kamal 1982; Pseudocercosporella meliae S.R. Chowdhury & Chandel 1986; Cercospora subsessilis var. azadirachtae R. Srivast. 1980 (FARR & ROSSMAN, 2011).
O fungo P. subsessilis pertence ao reino Fungi, divisão Ascomycota, classe Dothideomycetes, subclasse Dothideomycetidae, ordem Capnodiales, família Mycosphaerellaceae, gênero Pseudocercospora, espécie Pseudocercospora subsessilis (INDEX FUNGORUM, 2011).
Farr & Rossman (2011) apresenta em seu banco de dados 22 relatos de P. subsessilis ocorrendo em diferentes hospedeiros no mundo: infectando Azadirachta indica no Brasil (BRAUN & FREIRE, 2006); Hong Kong (LU et al., 2000); infectanto Azadirachta sp. em Hong Kong (ZHUANG, 2001); infectanto Melia azadirachta em Myanmar (THAUNG, 1984); infectanto Melia azedarach na China (GUO, 1995; GUO, 1999; ROUX et al., 1997; LU et al., 2000; LIU & GUO, 1998; ZHUANG, 2005), em Cuba (BRAUN & CASTANEDA-RUIZ, 1991), nos EUA (ALFIERI et al., 1984), em Hong Kong (LU et al., 2000; ZHUANG, 2001), na Índia (BAGYANARAYANA et al., 1991), em Taiwan (HSIEH & GOH, 1990), Tailândia (MEEBOON et al., 2007); infectando Melia azedarach var. subtripinnata no Japão (KOBAYASHI, 2007); infectando Melia sp. na China (GUO, 1999; ZHUANG, 2001; LIU & GUO, 1998); infectando Swietenia mahagoni nos EUA por ALFIERI et al. (1984).
Material de P. cedrelae (HCIO 26092) não estava disponível e não poderia ser comparado, mas um outro espécime capturado na Índia em cedrela Toona, foi comparado com P. subsessilis (Syd. & P. Syd.) Deighton, normalmente difundido em áreas tropicais e subtropicais, hospedando em Azadirachta sp., Melia sp. e Swietenia sp. E esse material é morfologicamente igual a P. cedrelae-mexicanae, mas difere em ter manchas nas folhas distintas com conspícua, bordas marrom e mais conídios, até 90 µm e com até 10 septos (BRAUN et al., 2003).
Diversos autores têm estudado os fungos cercosporóides do Brasil, iniciando-se com os estudos de Viégas (1945). Uma excelente compilação destaca as espécies descritas por Batista e colaboradores. Uma lista atualizada dos hifomicetos foi recentemente publicada, incluindo novos registros de fungos cercosporóides (FREIRE, 2005 apud FREIRE & BRAUN, 2009).
O objetivo deste trabalho foi identificar e registrar a ocorrência de cercosporiose em plantas de cinamomo na região de Urutaí, GO, descrevendo a respeito da sua sintomatologia, etiologia, epidemiologia e controle.
2. MATERIAIS E MÉTODOS
Amostras de folhas de Cinamomo (M. azedarach), com sintomas da doença, foram coletadas na área do Pivô do Instituto Federal Goiano, localizada no município de Urutaí - Goiás e encaminhadas para o Laboratório de Microbiologia.
Com auxílio do microscópio estereoscópico e uma lâmina especial, para realizar cortes, foram preparados cortes transversais do mesófilo foliar das folhas apresentando sinais do patógeno para observação da interação patógeno-planta e suas conseqüências.
Preparou-se lâminas semi-permanentes pelo método de “pescagem direta” para análise em microscópio óptico descrição morfológica e morfométrica das estruturas fúngicas. Usando uma lâmina com uma gota de fixador, raspou-se as estruturas das pústulas com auxílio de uma pinça foram feitas lâminas para visualização e posterior identificação do patógeno. Assim usou-se uma lâmina contendo uma lamínula a ser montada, vedada com esmalte e levada ao microscópio para visualização.
Após a visualização da lâmina em microscópio óptico, identificou-se as estruturas e através destas foi possível sua identificação. As estruturas do fungo foram posteriormente microfotografado com auxílio de uma câmera digital marca Canon modelo Power Shot SD750, do professor Milton Luiz da Paz Lima, sendo transferidas as imagens para um computador.
3. RESULTADOS E DISCUSSÃO
Hospedeiro/cultura: Cinamomo (Melia azedarach L.).Família Botânica: Meliaceae Doença: Cercosporiose (mancha foliar)Agente Causal: Pseudocercospora subsessilis Syd. & P. Syd. (Anamorfo), Mycosphaerella (Teleomorfo).Local de Coleta: Urutaí, GO. Data de Coleta: 07/2011Taxonomia: Reino Fungi, Divisão Ascomycota, Classe Dothideomycetes, Subclasse Dothideomycetidae, Ordem Capnodiales, Família Mycosphaerellaceae, Gênero Pseudocercospora sp., Espécie P. subsessilis.Sintomatologia As folhas, mais velhas, apresentaram as seguintes características: Sintomas: manchas foliares irregulares, anfígenas, angulares a circulares, coloração pardo-escura, de diâmetro de 0,5 a 3 mm (Fig. 1A). Os sinais são: anfígenos, centrais, localizados no centro da lesão (Fig. 1C) (BRUNHEROTTO & VENDRAMIM, 2001).
Etiologia
O isolado na forma anamórfica (P. subsessilis) apresentou conidióforo hialino, curtos, produzidos em abundante tecido estromático (emergência através da abertura estomatal) (Fig. 1D), simpodial, agrupados em fascículos, apresentou cicatrizes conidiais, ápice truncado possuindo dimensões de 47,5-(37,75)-25 x 4-5 µm (Fig. 1F); conídios cicatrizados, curvados, com 3-5 septos, truncados, escuros, medindo 37-(49)-52 x 4-5 µm (Fig. 1K.L.M.N). Sua forma de sobrevivência geralmente é em restos culturais ou em hospedeiros alternativos (A. indica) (CHUPP, 1953).
Etiologia
O isolado na forma anamórfica (P. subsessilis) apresentou conidióforo hialino, curtos, produzidos em abundante tecido estromático (emergência através da abertura estomatal) (Fig. 1D), simpodial, agrupados em fascículos, apresentou cicatrizes conidiais, ápice truncado possuindo dimensões de 47,5-(37,75)-25 x 4-5 µm (Fig. 1F); conídios cicatrizados, curvados, com 3-5 septos, truncados, escuros, medindo 37-(49)-52 x 4-5 µm (Fig. 1K.L.M.N). Sua forma de sobrevivência geralmente é em restos culturais ou em hospedeiros alternativos (A. indica) (CHUPP, 1953).
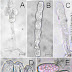
Figura 1. Cercosporiose (Psedocercospora subsessilis) em folhas de cinamomo (Melia azedarach) A. Sintoma de crestamento e manchas foliares nos folíolos apicais, B. Lesões necróticas esféricas e de coloração pálea na face abaxial, C. Detalhe dos sinais distribuídos uniformemente no centro da lesão, D. Tecido estromático (sinais) no centro da lesão na face adaxial, E. Corte histológico mostrando a interação patógeno-hospedeiro, F. Esporodóquio com conidióforo curto e detalhe para célula conidiogênica (seta) (bar=22,5µm), G. Tecido estomático esporodoquial e conídio (seta) preso a célula conidiogênica (bar=22,5µm), H. Conídio multisseptado e hialino (bar=5µm), I. Célula pé do conidióforo (seta) (bar=6,5µm), J. Célula conidiogênica curta(bar=6,5µm), K., L., M., N., Variação morfológica dos conídios multisseptados, hialinos, de base truncada e ápice agudo (bar=5µm).
Epidemiologia
A doença apresenta ampla dispersão geográfica, podendo ser encontrada desde as zonas temperadas até os trópicos (FREIRE & BRAUN, 2009). Umidade relativa próxima a 100% e temperaturas entre 15-30 °C são condições que favorecem o desenvolvimento da doença. Como características de cercosporioses, o fungo pode sobreviver nos restos de cultura infectados deixados no solo e nas sementes por mais de dois anos. Os conídios são disseminados a longa distância pelas sementes infectadas ou contaminadas. Na plantação, os conídios são dispersos pelo solo, vento, respingos da água da chuva ou da irrigação, operários e implementos de trabalho. No Brasil a ocorrência desse fungo só foi relatada para cultura do Nin (A. indica) sendo este o primeiro relato de P. subsessilis infectando Cinamomo (Melia azedarach). No mundo ela infesta as seguintes espécies: A. indica, Azadirachta sp., M. azadirachta, M. azedarach var subtripinnata, Melia sp., Swietenia mahagoni (FARR & ROSSMAN, 2011).
Controle
Não há relato de controle para P. subsessilis no Brasil, existe o controle para C. apii, que também infecta o Cinamomo, em batata aipo (Agrofit, 2011). A adoção deste controle requer alguns cuidados para o sucesso da aplicação e eficiência do controle, tais como: escolha do fungicida (contato ou sistêmico), horário da aplicação (fatores climáticos), forma da aplicação (jato dirigido ou pulverizado) e intervalos entre aplicações. Existem atualmente três produtos registrados no Ministério da Agricultura para o controle químico da cercosporiose (C. apii) que também infecta o Cinamomo: contact; garant; garant BR (hidróxido de cobre) (Agrofit, 2011). Apesar de o Cinamomo ser uma espécie usada também como forma de controle biológico, através do seu extrato, essa prática ainda não se aplica para a cultura, pois o seu efeito é apenas inseticida.
As cercosporioses têm como principal método de controle: o cultural, físico e o químico. Os principais aspectos de controle a serem relacionados são: o bom preparo do solo, o histórico da área a ser plantada visando o melhor manejo a ser implantado, a época do plantio, combate as plantas daninhas, que pode se hospedeiras de alguns fungos patogênicos, destruição de restos culturais entre outros (AMORIM et al., 2011).
LITERATURA CITADA
AGROFIT – Sistema de Agrotóxicos Fitosanitários. Disponível em: . Acessado em: 08/11/2011.
AMORIM, L.; REZENDE, J. A. M.; BERGAMIN FILHO, A.: Manual de Fitopatologia: Princípios e Conceitos: 4ª ed. Vol. 1, p 40; 510-515 - São Paulo, SP. Editora Agronômica Ceres Ltda., 2011.
BRAUN. U.; CROUS, P.; KAMAL.: New species of Pseudocercospora, Pseudocercosporella, Ramularia and Stenella. Mycological Progress 2(3): 197–208, August, 2003.
BRUNHEROTTO, R.; VENDRAMIM, J.D. Bioatividade de extratos aquosos de Melia azedarach L. sobre o desenvolvimento de Tuta absoluta (Meyrick) (Lepidoptera: Gelechiidae) em tomateiro. Neotropical Entomology, 30: 455-459, 2001.
CHUPP, C.: Monograph of the fungus genus Cercospora. Published by the Author, Ithaca, New York, 667 pages. 1953.
FARR, D.F., & ROSSMAN, A.Y. Fungal Databases, Systematic Mycology and Microbiology Laboratory, ARS, USDA. Retrieved November 1, 2011, from /fungaldatabases/. Disponível em: . acessado em: 01/11/2011.
FREIRE, F. D. C. O.; BRAUN, U.: Hifomicetos Cercosporioides Associados a Plantas do Estado do Ceará: Revista Ciência Agronômica, v.40, n.1, p. 150-156 jan-marc. Centro de Ciências Agrárias – Universidade Federal do Ceará, Fortaleza, CE, 2009.
INDEX FUNGORUM. Banco de Dados para Consulta de Táxons de Fungos. Disponível em: . Acessado em: 07/11/2011.
SOUSA NETTO, M.; OLIVEIRA, F.C. DE; PAZ-LIMA, M.L. Ocorrência de cercosporiose (Pseudocercospora subsessilis) em folhas de cinamomo (Melia azedarach). Tropical Plant Pathology. 36(supl.):756. 2011a.
SOUSA NETTO, M.; OLIVEIRA, F.C. DE; PAZ-LIMA, M.L. Ocorrência de cercosporiose (Pseudocercospora subsessilis) em folhas de cinamomo (Melia azedarach). Anais II Jornada de Iniciação Cientifica. Instituto Federal Goiano campus Urutaí - Urutaí, GO. 2011b.