Autores:
ANA FLÁVIA DE JESUS PINTO (1)
DÉBORA PIVA LIMA (2)
DIEGO
DE ALMEIDA (1)
FERNANDA
CORRÊA (1)
JADH
TAINÃ COSTA AQUINO (1)
LAYANE
YASMIM BERNARDES DINIZ (1)
RAÍSSA RODRIGUES CANEDO (2)
TONY DE LIMA (1)
Estudantes do Curso de Agronomia(1) e Tecnologia em Gestão Ambiental(2)
Urutaí, 19 de junho de 2013.
1. INTRODUÇÃO
O uso intensivo e inadequado das diversas áreas
exploradas tem contribuído para o declínio considerável da fertilidade natural
dos solos. Esse manejo inadequado tem contribuído para o processo de degradação
da matéria orgânica, causando perdas de algumas propriedades físicas, químicas
e biológicas, acelerando a erosão e diminuindo o potencial produtivo das
culturas (CALEGARI, 2000).
A
diversidade de microrganismos como indicador da qualidade do solo tem sido
bastante debatido, especialmente na última década, com o advento de técnicas de
biologia molecular que têm favorecido a avaliação dos microrganismos em
amostras ambientais (COUTINHO et al., 1999; ROSADO, 2000; TIEDJE et al., 2001).
O principal argumento a favor dessa característica ambiental é o fato da
diversidade microbiana manter-se naturalmente inalterada ao longo do ano (SMIT
et al., 2001; JOHNSON et al., 2003).
Vê-se,
dessa forma, que a diversidade de microrganismos é crítica para o funcionamento
do ecossistema, porque há a necessidade da manutenção de processos ecológicos
como a decomposição da matéria orgânica, ciclagem de nutrientes, agregação do
solo e controle de patógenos dentro do ecossistema (KENNEDY, 1999). Dessa
forma, é extremamente importante a busca de métodos de avaliação da diversidade
de microrganismos no solo e também de formas de utilização desses dados como
indicadores do estado da qualidade do solo.
Fungos e bactérias de solo são onipresentes no ambiente e
cumprem uma gama de funções ecológicas importantes, em
particular aqueles associados à mineralização de nutrientes no solo
( ANDERSON & CAIRNEY, 2004 ). Apesar disto, a compreensão
da dinâmica das populações de fungos de solo e bactérias
é um desafio, em especial fungos micorrízicos
arbusculares (FMAs), devido à dificuldade de cultivo e identificação
destes organismos. Estudos através de isolamentos em meios
de cultivo artificiais são difíceis de serem executados e
muitas vezes fornecem resultados não conclusivos. Entretanto
este desafio está sendo vencido com o auxílio de novas técnicas
baseadas no uso de marcadores moleculares. Recentes
investigações sobre a ecologia de fungos do solo estão sendo
realizadas através da extração do material genético diretamente
do solo ou de raízes colonizadas, o que tem trazido significativo
aumento na compreensão da diversidade de fungos em raízes de
plantas e/ou solo (SIQUEIRA & MOREIRA, 1999).
A fauna do solo tem um importante papel na regulação dos
sistemas agrícolas e, desde os anos 1980, vem sendo pesquisada no Brasil como
indicador de sustentabilidade do manejo dos solos tropicais. Tem importante
atuação nos processos de decomposição, mineralização e humificação de resíduos
orgânicos; imobilização e mobilização de macro e micronutrientes; fixação de
nitrogênio atmosférico; estruturação e agregação do solo e conseqüente conservação
e regulação de pragas e doenças (auto-regulação), beneficiando os sistemas de
produção como um todo (LAVELLE et al, 1997).
Alguns organismos da macrofauna, principalmente os térmitas,
as formigas, as minhocas e larvas de coleópteros, são denominados “engenheiros
do ecossistema”, pois suas atividades levam à criação de estruturas biogênicas
(galerias, ninhos, câmaras e bolotas fecais), que modificam as propriedades
físicas dos solos onde vivem e a disponibilidade de recursos para outros
organismos (WOLTERS, 2000). Por meio de suas ações mecânicas no solo, a
macrofauna contribui na formação de agregados estáveis, que podem proteger
parte da matéria orgânica de uma mineralização rápida e que constituem, também,
uma reserva de nutrientes potencialmente disponível para as plantas (LAVELLE
& SPAIN, 2001; DECÄENS et al., 2003).
A macrofauna é constituída por uma complexidade de organismos
que diferem no tamanho, metabolismo, atividades e mobilidade (PASINI E BENTO,
2004), com comprimento maior que 2 mm (SWIFT et al., 1979). Conforme Bayer e
Mielniczuk (1999), a macrofauna tem papel fundamental na fragmentação e
incorporação dos resíduos ao solo, criando assim, condições favoráveis à ação
decompositora dos microorganismos. Entretanto os benefícios da fauna edáfica
são poucos conhecidos em solos brasileiros (ALVES et al., 2006) apud Montenegro
et al. (2010).
O objetivo deste trabalho é quantificar a diversidade
microbiana e de macrorganismos em diferentes usos de solo na fazenda Pedra
Branca e Palmital.
2. MATERIAL E
MÉTODOS
O trabalho
foi conduzido nos dias 26 de março e no dia 2 de abril, no Instituto Federal de
Educação, Ciência e Tecnologia Goiano, IF Goiano – campus Urutaí, localizado no sudoeste goiano. As armadilhas foram
instaladas na área de mata, em pastagem e na área de pivô (cultivada).
Foram
utilizadas armadilhas do tipo “Pitfall” compostas de garrafas PET com
capacidade de 600 mL cortadas na região do gargalo, de modo que o fundo da
garrafa fosse enterrado e o orifício ficasse ao nível da superfície do solo. Em
cada ambiente, as armadilhas foram marcadas com estacas posteriormente
geo-referenciadas. Sobre as armadilhas foi colocada uma proteção, essa proteção
foi feita com bandejas de isopor e palitos de churrasco, em cada extremidade da
bandeja foi colocado um palito e eles foram fincados no solo, formando uma casa
para a garrafa pet. Em todas as áreas
foram colocados 5 pontos escolhidos aleatoriamente totalizando 20 amostras, 5
amostras de cada grupo.
Foram
coletadas aproximadamente 300 gramas de solo, em uma profundidade máxima de 20
cm, utilizando enxadão para a retirada das amostras e colocadas em sacos
plásticos e levadas ao Laboratório de Microbiologia. Onde foi realizada a
diluição em série. Vale ressaltar que a coleta foi realizada logo após uma
chuva.
Cada armadilha continha uma mistura de 100 mL
de solução etanol e detergente. Após sete dias a campo as armadilhas foram
coletadas e encaminhadas para o laboratório de microbiologia para posterior identificação
da macrofauna edáfica.
Para a
realização desse método, tomou-se 1 grama da amostra composta, pesada em
balança de precisão. Em seguida, essa amostra foi levada a câmara de fluxo
laminar, onde se realizou o restante dos procedimentos. Esta amostra foi
transferida para um tubo de ensaio, com o auxílio de pinça, contendo 9 mL de
solução salina esterilizada, tornando-se um solução diluída com concentração 10-1.
Logo em
seguida foi preparada a solução de 10-2, transferindo com uma pipeta
estéril, 1 mL da concentração 10-1, que foi agitada por
aproximadamente 30 segundo em agitador, para outro tubo de ensaio contendo 9 mL
de solução salina.
Foram
realizadas as diluições para as concentrações 10-3, 10-4
e 10-5, seguindo o mesmo procedimento realizado anteriormente, esse
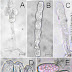
procedimento pode ser melhor compreendido de acordo com a Figura 1. Para a
determinação da densidade microbiana as concentrações de 10-1 e 10-2
foram descartadas.
Figura 1. Sequencia de atividade de diluição e plaqueamento utilizando o método de diluição em série para quantificação de densidade microbianas.
Logo após,
de ser feitas as diluições foi feita a semeadura, com a ponteira, de 1μL das
mesmas em placas de Petri contendo meio de cultura BDA, com duas repetições
para cada concentração. As placas foram vedadas e etiquetas e levadas à estufa
de crescimento biológico e deixadas por 48 horas à 35 oC.
Posteriormente,
foi realizada a contagem da Unidade Formadora de Colônias (ufc), de forma
visual, dividindo a placa em quadrantes. Na contagem foi levado em consideração
o número total de unidades formadoras de colônias. Em seguida foi realizado o
cálculo para determinação da densidade microbiana. O cálculo foi feito da
seguinte maneira: como o volume na placa de Petri era de 1 μL, foi necessário
encontrar o número de ufc/mL através de regra de três simples, este valor foi
multiplicado pelo índice de diluição da amostra.
O valor de ufc
encontrado nas placas de Petri foram submetidas à análise estatística
utilizando o software SAS. Foi realizado o teste paramétrico (ANOVA) e o teste
de Tukey. E quando submetidas à análise de significância as médias necessitaram
ser transformadas para melhorar a confiabilidade da análise.
O material
coletado foi lavado em peneira e com o auxílio de pinças, foi feita a contagem
e identificação da macrofauna, os organismos foram então, colocados em um vidro
contendo álcool.
Os
resultados obtidos foram submetidos à análise de variância usando o software SAS
e quando significativos (p<0 a="" aplica="" as="" avaliada="" baseado="" cies="" coeficiente="" compara="" da="" de="" dias="" diversidade="" do="" e="" entre="" esp="" fisher="" foi="" m="" meio="" ndices="" nos="" o="" p="" pela="" pelos="" por="" realizado="" riqueza="" shannon="" simpson="" software="" spade.="" teste="" tukey.="" utilizando="" valores="" varia="">
3. RESULTADOS E DISCUSSÃO
A comparação
da diversidade dos indivíduos da macrofauna presente nos demais ambientes: área
de mata, pastagens e área do pivô (cultivada) demonstrou uma grande variação de
grupos faunísticos, onde foram coletados 1613 indivíduos, pertencentes a vários
grupos taxonômicos. Observou-se um maior número de indivíduos da ordem dos Coleoptera
(besouros, vagalume), Hymenoptera (formiga, mariposas) e Orthoptera (grilo,
gafanhoto), o grupo de menor representante foi Hylidae (Perereca) onde se
encontrou 1 indivíduo.
Por causa da
grande área rizosférica e grande quantidade de matéria orgânica fornecida era
de ser esperar que a floresta apresentasse um grande de microrganismos. Mas a
área de culturas (pivô) apresentou se um maior número de ufc’s (Tabela 1).
Deve-se A diversidade vegetal, umidade, aeração e presença de uma vasta
rizosfera onde os microrganismos se desenvolvem e contribuem para um bom solo
onde se proporciona um substrato ideal para um crescimento de árvores,
gramíneas.
Média do
Número de Unidades Formadoras de Colônias por mL de solução do solo (ufc/mL) em
relação às diluições e as áreas.
Tabela 1. Média do
número de Unidades Formadoras de Colônias por mL de solução de solo (ufc/mL) em
relação às diluições.
Analisando as médias de ufc por cada
mL de solução do solo a densidade microbiana nos solos de culturas é superior.
A pequena diferença entre as médias em solo de cultivo e pastagem pode ser
explicada pelo uso contínuo de fertilizantes para o plantio e cobertura. Estes
fertilizantes possibilitam um maior número de nutrientes disponível as plantas,
melhorando, então, a rizosfera. Além disso, estes fertilizantes não deixam de
liberar nutrientes diretamente para o desenvolvimento de microrganismos.
Estatisticamente,
pelo teste F (ANOVA) a análise de variância é um procedimento utilizado para
comparar três ou mais tratamentos. Existem muitas variações da ANOVA devido aos
diferentes tipos de experimentos que podem ser realizados. A hipótese da
nulidade H0 foi rejeitada tanto a 1% quando a 5 % sendo o valor F
calculado maior que o valor F tabelado (Tabela 2), as médias se diferem entre
elas, portanto os tratamentos são diferentes.
Tabela 2. Teste paramétrico ANOVA das
médias do número de ufc transformadas encontradas nas diluições.
A diversidade biológica foi avaliada através da
aplicação dos índices de Shannon, Simpson e de Fisher, que mostram o domínio
dos grupos faunísticos nas áreas estudadas. O índice de Shannon mede o grau de
incerteza em prever a que espécie pertencerá um indivíduo escolhido ao acaso.
Quanto menor o valor do índice de Shannon, menor o grau de incerteza e,
portanto a diversidade da amostra é baixa. A diversidade tende a ser mais alta
quanto maior o valor do índice. Um parâmetro utilizado é a riqueza de espécies,
que diz pouco a respeito da organização da comunidade, mas serve com indicativo
de diversidade de organismos onde houve maior número na área da mata quando comparada
com a área de pivô que apresentou menor número de riqueza sendo o ambiente mais
desequilibrado das áreas pesquisadas.
Figura 2. Médias dos valores de riqueza de espécies nos diferentes
usos do solo (valores seguidos de mesma letra não diferem entre si pelo teste Tukey
a P~0,05).
O teste de Riqueza de Espécies (Figura 2), a
área de Floresta apresentou maior índice de 25.3, enquanto a pastagem 2
(Fazenda Palmital), culturas e pastagem 1 (Pedra Branca) apresentaram os seguintes valores 22.5; 10.2 e 4.1
respectivamente. Floresta e Pastagem 2 foi classificado “a” por apresentar um
grande número de organismos naquele espaço, onde pode ser considerados
estatisticamente iguais, já Culturas e Pastagem 1 foi classificado “b” por ressaltar diferença de organismos no ambiente assim sendo
diferentes da Floresta e Pastagem 2 .
Figura 3. Médias dos valores do índice de Shannon nos diferentes
usos do solo (valores seguidos de mesma letra não diferem entre si ao Teste
Tukey a P~0,05).
No índice de
Shannon (Figura 3) é observada a diversidade de espécies, onde se leva a
riqueza e a equabilidade em consideração. A floresta, pastagem 2 e cultura
(pivô) apresentaram os valores
respectivamente maiores do que a Pastagem1 que se diferencia por ter um menor índice.
Figura 4. Médias dos valores do índice de Simpson nos diferentes
usos do solo (valores seguidos de mesma letra não diferem entre si ao Teste
Tukey a P~0,05).
O Índice de
Simpson (Figura 4) também leva em
consideração a riqueza e a igualdade
como nos demais gráficos. Neste índice, a pastagem 1 obteve maior índice , pois
possui um número maior de indivíduos,
pois neste ambiente pode ser de um solo estável de bom desenvolvimento aos
organismos. Diferenciando dos demais índices pastagem 2, floresta e culturas
que estão menor mais são equivalentes.
Figura 5. Médias dos valores do índice de Fisher nos diferentes
usos do solo (valores seguidos de mesma letra não diferem entre si ao Teste
Tukey a P~0,05).
No Índice de Fisher (Figura 5) é analisada a relação do
número de espécies representadas por apenas 1 indivíduo na comunidade.
Novamente a área de floresta apresentou se uma maior média se
diferenciando dos demais tratamentos que
apresentaram médias como a pastagem 2, a área de cultura e a pastagem 1. Isso pode ser explicado pela
grande diversidade que a área de floresta apresenta, pois ela apresenta uma
vegetação mais diversificada, fornecendo maior matéria orgânica e conseqüentemente
um maior número de organismos interagindo no ambiente.
4. CONCLUSÃO
A
preservação de áreas florestais contribui para a existência de uma elevada
densidade microbiana no solo, devido a fatores favoráveis ao desenvolvimento
desse tipo de organismos. Em áreas que sofreram ações antrópicas essa densidade
é inferior, já que houve interferência nas propriedades físicas, químicas e na
diversidade vegetal do ambiente, cujas estão interligadas ao crescimento de
microrganismos no solo.
As áreas em
que foi feito a análise de ambientes diferentes como floresta, pastagem 1,
pastagem 2 e culturas era de se esperar que a área de floresta apresentasse
média superior de ufc e organismos comparadas as demais. Isso se deve a grande
biodiversidade das áreas preservadas, que pode ser explicado pela maior quantidade
de matéria orgânica oriunda da diversidade vegetal, umidade, aeração e presença
de uma vasta rizosfera, proporcionando um substrato ideal para o desenvolvimento
de microrganismos.
Mas isso não
ocorreu, a área de culturas apresentou um maior número de ufc e organismos, talvez
haja um fator de desequilíbrio onde tal espécie possa estar predominando no
momento, por falta de competição ou agentes que a controla, a contagem do número
de ufc também pode ter sido feita de maneira errônea em qualquer área estudada.
Outro fator que pode ter interferido no número de organismos encontrados na
área de pivô foi o fato de terem utilizado sacolas plásticas de cor amarela o
que chama atenção dos organismos.
Uma área
nativa constitui um sistema em equilíbrio e sofre pouco influências antrópicas
como os demais tratamentos e o não revolvimento do solo e a permanência dos
resíduos possibilitam melhor desenvolvimento dos microrganismos, principalmente
devido ao aumento dos teores de matéria orgânica nas camadas mais superficiais.
Nas áreas de cultura e pastagem há o uso de fertilizantes para plantio, o que
permite um maior número de nutrientes disponível para as plantas. Também se
percebe que o tipo de manejo, seja ele um plantio direto com milho ou uma
pastagem não interfere na densidade microbiana entre os solos desses ambientes.
5. LITERATURA CITADA
ALVES, M. V.; BARETTA, D.;
CARDOSO, E. J. B. N. Fauna edáfica em diferentes sistemas de cultivo no estado
de São Paulo. Revista de Ciências Agroveterinárias, Lages, v.5, n.1, p.34,
2006;
ANDERSON, I.C.; CAIRNEY, W.G. Diversity and ecology
of soil fungal communities: increased understand though the apllication of
molecular techniques. Applied and
Environmental Microbiology, v. 6(8), p. 769-779, 2004.
BAYER, C.; MIELNICZUK, J.
Dinâmica e função da matéria orgânica. In: SANTOS, G. A.; CAMARGO, F. A. O.
Fundamentos da matéria orgânica do solo: ecossistemas tropicais e subtropicais.
Porto Alegre: Gênesis, Cap.2, p.9-26. 1999;
CALEGARI, A. Coberturas verdes
em sistemas intensivos de produção. In: Anais do Workshop Nitrogênio na
sustentabilidade de sistemas intensivos de produção agropecuária. EMBRAPA Agropecuária
Oeste/Agrobiologia. Dourados-MS, 2000. p. 141-153.
COUTINHO, H. L. da C.;
OLIVEIRA., V. M. de; MANFIO, G. P.; ROSADO, A. S. Evaluating the microbial
diversity of soil samples: methodological innovations. Anais da Academia Brasileira de Ciências, Rio de Janeiro, v. 71, n.
3, p. 491-503, 1999.
DECÄENS, T.; LAVELLE, P.;
JIMÉNEZ, J.J.; ESCOBAR, G.; RIPPSTEIN, G.; SCHNEIDMADL, J.; SANZ, J.I.; HOYOS,
P.; THOMAS, R.J. Impacto del uso de la tierra en la macrofauna del suelo de los
Llanos Orientales de Colombia. In: JIMÉNEZ, J.J.; THOMAS, R.J. (Ed.). El arado
natural: las comunidades de macroinvertebrados del suelo en las savanas
neotropicales de Colombia. Cali, Colombia: Centro Internacional de Agricultura
Tropical, 2003. p.21-45. (Publicación CIAT, 336).
KENNEDY, A. C. Bacterial diversity in
agroecosystems. Agriculture, Ecosystems and
Environment, Amsterdam, v. 74, n. 1, p. 65-76, 1999.
LAVELLE, P ;et al Soil function in a changing
world: the role of invertebrate ecosystem engineers. European Journal of Soil
Biology, v.33, p.159–193, 1997.
LAVELLE, P. ; SPAIN, A.V. Soil ecology. Dordrecht: Kluwer Academic Pub., 2001. 654p.
MONTENEGRO, F. T. ; SOUZA;
G. A.
V. S. ; OLIVEIRA, J. C. Levantamento
da macrofauna edáfica na cultura da mamoneira (Ricinus communis l.) no
município de lagoa seca-PB. CONGRESSO BRASILEIRO DE MAMONA, 4 & SIMPÓSIO
INTERNACIONAL DE OLEAGINOSAS ENERGÉTICAS, 1, 2010, João Pessoa. Inclusão Social
e Energia: Anais... Campina grande: Embrapa Algodão, 2010. p. 1002-1007.
PASINI, A.; BENTO, N. P. Macrofauna do Solo em Agroecossistemas.
In: FERTBIO, Lages, Anais… Lages, SBCS, 2004.CD-ROM;
SIQUEIRA, J. O.; et al.
Inter.relação fertilidade, biologia do solo e nutrição de plantas, Lavras, MG.
1999.
SMIT, E.; LEEFLANG, P.; GOMMANS, S.; VAN DEN
BROEK, J.; VAN, M. S.; WERNARS, K. Diversity and seasonal fluctuations of the
dominant members of the bacterial soil community in a wheat field as determined
by cultivation and molecular methods. Applied
and Environmental Microbiology, Washington, v. 67, n. 5, p. 2284-2291,
2001.
SWIFT, M. J.; HEAL, O. W.; ANDERSON, J. M. Decomposition in terrestrial ecosystems.
Berkeley: University of California Press, p. 66-117. 1979.
TIEDJE, J. M.; CHO, J. C.; MURRAY, A.; TREVES,
D.; XIA, B.; AHOU, J. Soil teeming with life: new frontiers for soil science.
In: REES, R. M.; BALL, B. C.; CAMPEBELL, C. D.; WATSON, C. A. (Org.).
Sustainable management of soil organic matter. Wallingford: CAB International,
2001. p. 393-412.
WOLTERS, V. Invertebrate control of soil
organic matter stability. Biology and Fertility of Soils, v.31, p.1-19,
2000.