ANTRACNOSE DA
BERINJELA (Solanum melongena) CAUSADA
POR Colletotrichum acutatum
Caio César de Oliveira Pereira
Acadêmico do curso de
Agronomia
INTRODUÇÃO
A berinjela (Solanum
melongena L. – Solanaceae) assim como o tomate, pimenta, pimentão,
batata e jiló. Foi introduzida à dieta brasileira por emigrantes árabes, sendo
consumida principalmente nos estados de São Paulo, Rio de Janeiro e Paraná (EMBRAPA
HORTALIÇAS, 2007). Os frutos cozidos são usados como verdura ou hortaliça nos
trópicos. Podem, também, ser fervidos, fritos, recheados, grelhados ou
refogados. As variedades que apresentam frutos pequenos baby são utilizadas
para produção de conservas/picles. Os frutos imaturos são, algumas vezes,
utilizados em molhos (PURSEGLOVE, 1968).
O gênero Solanum é
predominantemente originário das Américas Central e do Sul (cerca de 2.000
espécies), porém existem apenas cerca de 40 espécies nativas da Ásia, e entre
elas, 27 na Índia englobando a berinjela e seus parentes silvestres. Embora não
tenha sido completamente elucidada ainda, a maior parte das evidências indica
que a berinjela teve origem na Ásia. Regiões como o Oriente Médio, a região
Indo-Burma, Japão e China têm sido indicadas como prováveis centros de origem
por diversos autores. Entretanto, mesmo tendo-se registros de cultivo há mais de
1500 anos, em determinadas regiões da China, Khan (1979) e Kalloo (1993)
consideram a Índia como provável lugar de origem da berinjela, devido às
inúmeras referências encontradas em documentos escritos em sânscrito, linguagem
ancestral desse país. Martin e Pollack (1979) consideram a China e África como
centros secundários de dispersão.
A berinjela é uma das espécies mais rústicas entre as hortaliças. Mesmos
assim, é suscetível a algumas doenças que podem causar perdas consideráveis ou
comprometer a qualidade do produto, dependendo da cultivar, da época de cultivo
e das condições ambientais prevalecentes no local do plantio (RIBEIRO, 1998).
No campo, as murchas, provocadas por vários patógenos, são as mais
evidentes e as que mais preocupam o produtor, pois provocam perdas diretas e
ainda comprometem o terreno para cultivos posteriores, não somente da
berinjela, mas de espécies da mesma família. Em cultivos sob proteção de
plástico ou telado, essas doenças são mais importantes pelo fato de a rotação
de culturas, recomendada para todas elas, ser mais difícil por questões
econômicas. Além disso, as condições de temperatura e umidade, normalmente mais
elevadas do que a céu aberto, e menor ventilação, poderão interferir
negativamente na ocorrência também nas doenças foliares e no seu manejo (RIBEIRO,
1998).
Segundo Ribeiro (1998), as doenças e seus agentes causais, mais
importantes da berinjela no Brasil são listadas, respectivamente, a seguir, em
ordem cronológica de acordo com o ciclo da cultura: Doenças do solo: Tombamento ou 'damping-off' (Rhizoctonia
solani J.G. Kühn, Pythium spp.
Pringsh., Phytophthora spp. Bary);
Murcha-de-verticílio (Verticillium
dahliae Kleb.); Murcha-bacteriana
ou murchadeira (Ralstonia solanacearum Smith); Murcha-de-Fitóftora
(Phytophthora capsici Leonian); Podridão-de-esclerotínia (Sclerotinia sclerotiorum (Lib.)
de Bary); Podridão-de-esclerócio (Sclerotium rolfsii Sacc.); Nematóide-das-galhas (Meloidogyne spp.); Doenças da parte aérea: Podridão-de-fomopsis
ou seca-dos-ramos (Phomopsis
vexans (Sacc. & P. Syd.)
Harter); Antracnose (Colletotrichum
gloeosporioides (Penz.)
Penz. & Sacc.); Podridão-algodão (Phytophthora nicotianae Breda
de Haan, P. capsici ou Pythium spp.); Ferrugem (Puccinia sp. Pers.); Oídio (Oidiopsis haplophylli (Magnus) Rulamort); Podridão-mole (Erwinia carotovora); Pinta-preta
ou mancha-de-alternária (Alternaria
solani (Ellis & G. Martin) L.R. Jones & Grout); Mancha-bacteriana (Xanthomonas spp.); Superbrotamento;
Mosaico (vírus do gênero Potyvirus); Vira-cabeça vírus do
gênero Tospovírus).
O fungo Colletotrichum
acutatum J.H. Simmonds (INDEX FUNGORUM, 2015) é uma das espécies mais
frequentemente relatadas do gênero e causa doenças comumente conhecidas como
antracnose em todo o mundo (FARR & ROSSMAN, 2015). Originalmente descrita a
partir de tecidos doentes de Carica papaya
L., Capsicum frutescens L. e Delphinium ajacis L. na Austrália por
Simmonds (1965), o complexo de espécies C.
acutatum é hoje conhecido como especialmente destrutivo em frutas como morango
(GARRIDO, 2009), citros (PERES et al.,
2008), maçã (LEE, 2007), azeitona (TALHINHAS, 2011) e mirtilo (WHARTON &
SCHILDER, 2008). Há também relatos de uma infecção disseminada em uma tartaruga
marinha (MANIRE, 2002) e a infecção de um cochonilha-de-carapaça (MARCELINO,
2008). Avaliações da espécie em seu sentido mais amplo e sua patologia, foram
publicadas por Wharton & Diéguez-Uribeondo (2004) e Peres et al. (2005).
No morango, C. acutatum
causa principalmente mancha preta dos frutos, mas também pode atacar coroas,
raízes e folhas (FREEMAN & KATAN, 1997), e é uma das doenças mais graves em
produção de frutos comerciais. Em grande parte, devido à sua importância
econômica como um patógeno do morango, C.
acutatum foi tratado por muitos anos como uma praga quarentenária regulamentada
pela Organização Europeia e Mediterrânica para a Proteção das Plantas (EPPO),
embora ele está ausente da lista atual (EPPO, 2015) - presumivelmente devido a
sua distribuição agora difundido na Europa. Fontes de inóculo são frequentemente
material transplantado, principalmente com infecções quiescentes (RAHMAN &
LOUWS, 2008), plantas infectadas, ervas daninhas e outros hospedeiros (MCINNES,
1992; PARIKKA, 2006), enquanto a taxa de sobrevivência de conídios em solo de
campo natural é baixa (FREEMAN, 2002).
Guerber & Correl (2001) descreveram Glomerella acutata, a metamorfose sexual de C. acutatum, como o produto de experiências de acasalamento,
enquanto algumas espécies relacionadas são homotálicas, incluindo G. acutata var. fioriniae (MARCELINO, 2008), mais tarde considerado como uma
espécie separada C. fioriniae (SHIVAS
& TAN, 2009) e um isolado de uma espécie Glomerella relacionadas com C.
acutata da Acer platanoides nos
EUA (LOBUGLIO & PFISTER, 2008). Talgo et
al. (2007) observaram a metamorfose sexual de G. acutata em frutos de mirtilo naturalmente infectados na Noruega.
Numerosos estudos demonstraram que a C.
acutatum é morfologicamente e filogeneticamente diverso (SREENIVASAPRASAD, 1994;
JOHNSTON & JONES 1997; LARDNER, 1999; FREEMAN, 2001ª; NIRENBER, 2002;
TALHINHAS, 2002; GUERBER, 2003; LUBBE, 2004; DU, 2005; PERES, 2005;
SREENIVASAPRASAD & TALHINHAS, 2005; TALHINHAS, 2005; JOHNSTON, 2008). Sreenivasaprasad
et al. (1996) foram os primeiros a
reconhecer que C. acutatum era extraordinariamente
diversificado, com estirpes mostrando divergência de 5,8% na sequência ITS-1 em
comparação com os níveis de 2-4% frequentemente encontrados dentro de outras
espécies de fungos.
Objetivo
O
objetivo deste boletim técnico é descrever a sintomatologia, etiologia,
epidemiologia e controle da antracnose da berinjela causada por Colletotrichum acutatum.
DESENVOLVIMENTO
Hospedeiro/cultura: Berinjela (Solanum melongena L.)
Família Botânica: Solanaceae
Doença: Antracnose
Agente Causal: Colletotrichum
acutatum J.H.
Simmonds
Local de Coleta: Urutaí, Goiás
Data de Coleta: 21/03/15
Taxonomia: A fase teleomórfica pertence ao reino Fungi, filo
Ascomycota, sub-filo Pezizomycotina, classe Sordariomycetes, subclasse
Sordariomycetidae, família Glomerellaceae, gênero Glomerella sp., espécie G.
cingulata. A fase anamórfica pertence ao Reino Fungi, grupo inserto dos
fungos Mitospóricos, sub-grupo dos Coelomicetos, gênero Colletotrichum sp., espécie C.
acutatum.
Sintomatologia:
Os sintomas da antracnose são observados principalmente nos frutos, no
campo ou após a colheita. São caracterizados por áreas mais ou menos circulares.
Quando os sintomas são mais severos, aparecem pequenas lesões deprimidas,
encharcadas, de coloração marrom-clara podendo coalescer resultando em uma
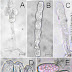
grande mancha de formato irregular (Fig. 1A). Em local com alta umidade, uma
massa de esporos de coloração rosada a salmão desenvolve-se sobre o centro da
lesão. Quando frutos novos aumentam em tamanho a superfície da lesão rompe-se, pois,
a área atacada não acompanha esse crescimento. Em caso mais severo, os frutos
tornam-se mumificados e pretos. Frutos atacados normalmente apodrecem (JUNQUEIRA,
2001; PICCININ et al., 2005; LIM
& MANICOM, 2003; PEREIRA & MARTINEZ JR,1986).
O fruto utilizado neste boletim técnico tinha uma severidade entre 5 a 10%
da área total. Possuía nove lesões deprimidas, de formato circular a elipsoide e
massa de esporos, de coloração salmão. Duas destas lesões não apresentavam
massa de esporos evidente. A maior
(Fig. 1B) e menor lesão, respectivamente, tinham as dimensões de 3,0-5,0 cm x 1,5-0,7 cm. O fruto apodreceu, acontecimento ocorrido num período de aproximadamente um mês, o mesmo é dependente de condições favoráveis do ambiente.
(Fig. 1B) e menor lesão, respectivamente, tinham as dimensões de 3,0-5,0 cm x 1,5-0,7 cm. O fruto apodreceu, acontecimento ocorrido num período de aproximadamente um mês, o mesmo é dependente de condições favoráveis do ambiente.
Etiologia (Sinais):
A característica morfológica mais conhecida do C. acutatum (sensu latu)
é a forma de seus conídios, que têm extremidades agudas (SIMMONDS, 1965). No
entanto, outras formas conidiais, especialmente ± cilíndrica com apenas uma
extremidade aguda, são frequentemente encontradas, especialmente nas estirpes
que foram repetidamente sub cultivada, mas estas formas conidiais também pode
ocorrer em espécies fora do complexo de espécies de C. acutatum. Mesmo a diferenciação entre C. acutatum (sensu latu)
e C. gloeosporioides (sensu latu) é difícil, porque muitas
cepas intermediárias existir com um número restrito de conídios fusiformes
típicas e muitos outros cilíndricos (VAN DER AA, 1990). No hospedeiro, conídios
são formados em acérvulos; em cultura, os conídios são também muitas vezes
produzidos no micélio aéreo (JOHNSTON & JONES, 1997). C. acutatum também foi observado formando conídios secundário sobre
a superfície das folhas de morangueiro vivos (LEANDRO, 2001) que foram
estimuladas por extratos de plantas de morango, especialmente extratos de
flores (LEANDRO, 2003). Buddie et al.
(1999) dizem que os conídios secundários podem ser produzidos diretamente a
partir da germinação de conídios primários, e são menores e mais variáveis em
forma, ocultando assim diferenças entre táxons. Além disso, C. acutatum formas apressórios
pigmentados simples, mas com pouca ou nenhuma seta (SIMMONDS, 1965).
Possui colônias efusas, brancas
tornando-se laranja pálido em seguida cinza esverdeado ou preta. Em placas os
versos das colônias, frequentemente, vão de rosa a púrpura avermelhado. Micélio
superficial, imerso, ramificado, septado, hialino a marrom escuro [feo].
Conidiomata [acérvulo] (Fig. 1E) usualmente ausente em meio de cultura (Fig.
1D). Seta ausente. Conidióforos hialinos, septados, ramificados com menor
frequência próximo a base, lisos. Células conidiogênicas fialídicas, hialinas,
lisas, cilíndricas, integradas, colaretes normalmente presentes, espessamento
periclinal presente. Conídio (Fig. 1FG) hialino, não septado, reto, liso,
fusiforme, 8-16 x 2,5-4 µm; Massa de esporos (Fig. 1AB) de coloração salmão.
Apressórios pouco numerosos, muitas vezes claro ao castanho médio, clavados a
oboclavados, margens lisas, apoia em hifas indiferenciadas 6,5-11 x 4,5-7,04 µm.
Em substrato natural: Acérvulo (Fig. 1E), superficial a subcuticular, composto
por textura angularis hialina; deiscência irregular, apresenta 0,5 mm diâmetro.
Setas presentes em algumas coleções, marrons (WALLER & SUTTON, 1979).
Tabela 1. Tabela
comparativa dos elementos morfológicos e morfométricos de C. acutatum com características descritas por Sutton (1979).
Características
|
Isolado Urutaí (2015)
|
Sutton (1992)
|
Cor da colônia
|
acinzentada
|
branco-gelo a cinza escuro
|
Cor da massa de
conídios
|
salmão
|
laranja pálido
|
Presença de acérvulo
|
presente
|
presente
|
Presença de seta
|
ausente
|
ausente
|
Características conidióforo:
|
||
Coloração
|
hialino
|
hialino
|
Característica
conídio:
|
||
Coloração
|
hialino
|
hialino
|
Forma
|
fusiforme
|
fusiforme
|
Presença
de gútula
|
presente (3)
|
nd
|
Dimensões
(µm)
|
8,24-(12,56)-15,63 x 2,53-(3,68)-5,51
|
8-16 x 2,5-4
|
Epidemiologia:
A antracnose possui como agente causal o fungo pertencente ao
gênero Colletotrichum sp. e
pode ser altamente devastadora, proporcionando perdas de até 100% na produção
quando os fatores cultivar suscetível, ambiente favorável ao patógeno e
sementes infectadas estiverem simultaneamente presentes durante o período de
cultivo (SILVA, 2004). A disseminação de planta a planta se dá principalmente
através dos respingos de chuva, pois os conídios estão aglutinados por uma
substância gelatinosa hidrossolúvel e não são facilmente carregados pelo vento.
Os conídios uma vez em contato com o hospedeiro, sob condições de umidade,
germinam e o pro-micélio resultante, com prévia formação de apressório, penetra
diretamente através da cutícula pela emissão do tubo de infecção (GALLI, 1978).
É comumente ocasionada pelo patógeno C.
gloeosporioides (Penz.) Penz & Sacc. 1884, apresentando uma
distribuição mundial e tem registro de 2101 hospedeiros (FARR & ROSSMAN,
2015).
Destes, o C. gloeosporioides
tem incidência em quatro espécies do gênero Solanum
– S. gilo Raddi (Brasil); S. melongena (Brasil,
Cuba, EUA, Porto Rico, Tailândia, Ilhas Virgens); S. melongena var. esculentum
(Dunal) Nees (Canada); S. tuberosum L.
(EUA).
A hospedeira berinjela possui 44 ocorrências ao redor do mundo,
ocasionadas por 12 espécies do gênero Colletotrichum
sp., onde temos três destas ocorrências registradas no Brasil e como suas
respectivas espécies: C. coccodes, C. gloeosporioides e Colletotrichum sp. (MENDES, 1998).
Sendo, assim, este boletim técnico é de grande valia, pois, apresenta o
primeiro registro de ocorrência de C.
acutatum em berinjela.
A espécie C. acutatum, agente causal estudado neste boletim técnico também
apresenta uma distribuição mundial e com 378 registros de patogenicidade (FARR
& ROSSMAN, 2015). Destes, a espécie tem 170 plantas hospedeiras
confirmadas. Sua forma teleomórfica G.
acutata, possui 8 hospedeiras, com 8 registros distintos de patogenicidade
(Fig. 1C), representados por Capsicum sp.,
China (XIA et al., 2011); Dactylis glomerata L., Espanha (SANCHEZ MARQUEZ et al., 2007); Fragaria sp., China
(XIA et al., 2011); Hakea sericea Schrad. & J.C.Wendl, Africa do Sul (YANG et al., 2009); Malus sp., China (XIA
et al., 2011); Olea europaea L., Africa
do Sul (THAN et al., 2008); Persea americana Mill, México (AVILA-QUEZADA et al., 2007); Vaccinium
corymbosum L., Noruega (TALGO et al.,
2007). Considerado um parasita cosmopolita.
O gênero é favorecido por
temperaturas elevadas, sendo a temperatura ótima entre 22 e 25°C, além de
necessitar de alta temperatura. Para que os esporos germinem, água livre deve
estar disponível. As temperaturas ótimas para germinação de conídios e formação
de apressórios estão entre 22 e 23°C. Os esporos somente são liberados dos
acérvulos quando estes encontram abundância de umidade. Respingos de chuva são
comuns meios de disseminação. Luz solar, baixa umidade e temperaturas extremas
(abaixo de 18°C ou superior a 28°C) inativa os esporos rapidamente (PONTE,
1996; PICCININ et al., 2005; MORAS,
2009).
Em meio de cultura, Colletotrichum forma colônias variáveis,
de coloração branco-gelo a cinza escuro, com quantidade variável de micélio
aéreo. É variável também a produção de estruturas reprodutivas em meio de
cultura (SUTTON, 1979)
C.
acutatum apresenta temperatura ótima de crescimento micelial compreendida
entre 25 e 26,5°C. A taxa de crescimento micelial de C. acutatum geralmente é mais lenta que a taxa de crescimento em C. gloeosporioides, e parece ser uma
característica cultural estável e de grande utilidade para separação das duas
espécies (VINNERE, 2004).
Controle:
O controle para a antracnose, causada por C. acutatum, em berinjela é de difícil manejo, sendo que o mesmo
não é um patógeno chave para a cultura. A berinjela tem como patógeno mais
comum a espécie C. gloeosporioides. C. acutatum é praga comumente
relacionada, no Brasil, aos citros. Através deste exposto, foram feitas
considerações para um manejo da antracnose em berinjela tentando fazer os
devidos ajustes tanto ao agente causal como ao hospedeiro:
Controle
biológico: A utilização através dos agentes de controle biológico
representados por B. subtilis e Trichoderma spp., assim como o
emprego de biofertilizantes, isoladamente ou em combinação com ACBs, mostram-se
como estratégias promissoras para o controle de C. acutatum, já que inibem a sua germinação conidial, suprimem a
produção de sintomas em flores de lima-ácida 'Tahiti' destacadas e propiciam a
obtenção de maior produtividade, representada pelo número médio de frutos
efetivos (KUPPER et al., 2009).
Controle físico: O emprego
da irradiação de alimentos no Brasil é muito promissor, com bons resultados na
redução das perdas pós-colheita (LIMA et al.,
2001). O processo de irradiação foi descrito por O´Beirne (1989) como o
uso de raios gama em alimentos, sem que haja risco de contaminação radioativa. Através
desta técnica foi verificada redução das lesões nas frutas tratadas com doses
de 0,45 kGy de radiação constatando que os tratamentos físicos não causaram
alterações significativas nas propriedades físico-químicas nos frutos tratados
(SANTOS, 2011).
Controle químico: O tratamento
químico também é uma alternativa viável de controle. Ao analisarmos e
compararmos os produtos formulados para a berinjela, agente causal C. gloeosporioides, com os produtos
formulados específicos do C. acutatum,
usualmente utilizados para citros, observamos um grupo químico bastante
utilizado para a berinjela: benzimidazol. O mesmo tem por ingrediente ativo o
carbendazim, para C. acutatum - marca
comercial Delsene WQ (Du Pont do Brasil S.A. - Barueri (Alphaville)) -, e o
tiofanato-metílico, para C.
gloeosporioides, - marcas comerciais Cercobin 700 WP (Iharabras S.A. Indústria
Químicas), Metiltiofan (Sipcam Nichino Brasil S.A. - Uberaba/MG), TOPSIN 700
(Iharabras S.A. Indústria Químicas), Viper 500 SC (Iharabras S.A. Indústria
Químicas), Viper 700 (Iharabras S.A. Indústria Químicas). Os demais produtos
utilizados para a cultura da berinjela, C.
gloeosporioides, levam como base do ingrediente ativo o elemento cobre
(Cu), e para o C. acutatum a apenas
um produto que leva tal elemento, representado por Starky (Laboratórios Pfizer
Ltda.) ingrediente ativo sulfato tribásico de cobre, grupo químico inorgânico
(AGROFIT, 2015).
Controle genético: No caso da
berinjela, sofrendo ataques do patógeno C.
gloeosporioides, pode-se utilizar cultivares resistentes tais como o
híbrido Ciça (REIFSCHNEIDER et al.,
1993). Também comentado por Madeira (1989) a antracnose teve sua importância
reduzida devido ao uso de cultivares com níveis mais elevados de resistência,
já que em cultivares suscetíveis, a frequência de frutos sintomáticos pode
variar de 35-100 %. Assim, o uso de cultivares resistentes, pode ser uma medida
que também tem condições de trazer resultado por minimizar os custos de
produção e reduzir os danos causados ao ambiente (SILVA, 2004).
Controle
cultural: Waller e Sutton (1979) dizem que a transmissão do fungo se dá por
conídios por via aérea, que o patógeno também pode ser transmitido por sementes
contaminadas e sobreviver em restos culturais. Então a utilização de cordões de
vegetação, usando árvores que não são hospedeiras conhecidas para o patógeno,
são de grande valia, assim como a queima dos restos culturais e a eliminação no
campo de partes e/ou plantas contaminadas. O uso de sementes sadias e rotação
de cultura também é um manejo que dá vantagens ao produtor sobre a doença.
AGROFIT. Sistemas de
Agrotóxicos Fitossanitários. Disponível em: ,
acesso em: 21 junho 2015.
AVILA-QUEZADA, G., SILVA-ROJAS, H.V.,
TELIZ-ORTIZ, D. First Report of the Anamorph of Glomerella
acutata Causing Anthracnose on Avocado Fruits in Mexico. Pl. Dis. 91: 1200, 2007
BUDDIE, A.,
MARTÍNEZ-CULEBRAS P., BRIDGE P., GARCÍA M., QUEROL A., CANNON P., MONTE E.
Molecular characterization of Colletotrichum strains derived
from strawberry. Mycological Research;
103(4):385–394. doi:
10.1017/S0953756298007254, 1999
DU, M., SCHARDL, CL., VAILLANCOURT, L.J. Using
mating-type gene sequences for improved phylogenetic resolution of Colletotrichum species
complexes. Mycologia 97: 641–658 2005
EMBRAPA HORTALIÇAS. Sistemas de
Produção, publicado em Nov./2007. Disponivel
em:,
acesso 09 de junho de 2015.
EPPO. EPPO A1 and A2 Lists of Pests
Recommended for Regulation as Quarantine Pests. EPPO,
Paris, FR, Disponível em: < http://www.eppo.int/>,
acessado em 20 junho de 2015
FARR, D.F., ROSSMAN, A.Y., SBML Systematic Botany of Mycological
Resources. Disponível em: <
http://nt.ars-grin.gov/fungaldatabases/>, acesso em 13 de abril de
2015.
FREEMAN,
S., HOROWITZ, S., SHARON, A. Pathogenic and
non-pathogenic lifestyles in Colletotrichum acutatum from
strawberry and other plants. Phytopathology 91: 986–992
2001a
FREEMAN,
S., KATAN, T. Identification of Colletotrichum species
responsible for anthracnose and root necrosis of strawberry in Israel. Phytopathology 87: 516–521,
1997
FREEMAN,
S., SHALEV, Z., KATAN, T. Survival in
soil of Colletotrichum acutatum and C. gloeosporioides pathogenic on
strrawberry. Plant
Disease 86: 965–970, 2002
GALLI,
FERDINANDO. Manual de Fitopatologia vol.2: doenças das plantas cultivadas.
4.ed. São Paulo: editora Agronômica Ceres, 1978.
GARRIDO, C., CARBÚ, M., FERNÁNDEZ-ACERO, F.J., VALLEJO,
I., CANTORAL, J.M. Phylogenetic relationships and
genome organization of Colletotrichum
acutatum causing anthracnose in strawberry. European Journal of Plant Pathology 125: 397–411,
2009
GUERBER,
J.C., CORRELL, J.C. (2001). Characterization
of Glomerella acutata, the
teleomorph of Colletotrichum acutatum. Mycologia 93: 216–229,
2001
GUERBER,
J.C., CORRELL, J.C. The first
report of the teleomorph of Colletotrichum acutatum in the United
States. Plant Disease 81: 1334,
1997
GUERBER, J.C., LIU, B., CORRELL, J.C., JOHNSTON, P.R. Characterization
of diversity in Colletotrichum
acutatum sensu lato by sequence analysis of two gene introns, mtDNA and intron
INDEX FUNGORUM. Disponível em: < http://www.indexfungorum.org/names/Names.asp>,
acesso em 13 abril 2015
JOHNSTON,
P., DODD, S., PARK, D., MASSEY, B., CHARUCHINDA, B. Are stable,
consistant, reliable and useful species names possible within Colletotrichum? In: Colletotrichum Diseases of Fruit
Crops (Peres NA, Timmer LW, editors., eds). Pre-Congress workshop, ICPP 2008,
August 24, Torino, Italy: 1–7, 2008
JOHNSTON,
P.R., JONES, D.Relationships among Colletotrichum isolates from
fruit-rots assessed using rDNA sequences. Mycologia 89: 420–430, 1997
JUNQUEIRA, N.T.V.; ANDRADE, L.R.M.;
PEREIRA, M.; LIMA, M.M.; CHAVES, R.C. Doenças da goiabeira no Cerrado.
Planaltina: Embrapa Cerrados, 2001. 31 p. (circular Técnica, 15)
KALLOO, G. Eggplant – Solanum melongena L. In: KALLOO, G. ; BERGH, B. O. Genetic Improvement of vegetable
crops. Oxford: Pergamon
Press. 1993. p. 587-604.
KHAN, R. Solanum melongena and
its ancestral forms. In: HAWKES, J. G.; LESTER, R. N.; SKELDING, A. D. (Ed.). Solanaceae I. The Biology and
Taxonomy of the Solanaceae. New York: Academic Press, 1979. p. 629-636.
KUPPER, K. C.; BELLOTTE, J. A. M.; GOES, A.
Controle alternativo de Colletotrichum
acutatum agente causal da queda prematura dos frutos cítricos. Revista
Brasileira de Fruticultura, v.31, no.4 Jaboticabal Dec. 2009.
LARDNER, R., JOHNSTON, P.R., PLUMMER, K.M., PEARSON, M.N. Morphological
and molecular analysis ofColletotrichum acutatum sensu lato. Mycological Research 103, 275–285,
1999
LEANDRO,
L.F.S., GLEASON, M.L., NUTTER, F.W. JR, WEGULO, S.N., DIXON, P.M. Strawberry plant
extracts stimulate secondary conidiation by Colletotrichum acutatum on symptomless
leaves. Phytopathology93:
1285–1291, 2003
LEANDRO,
L.F.S., GLEASON, M.L., NUTTER, F.W., JR., WEGULO, S.N., DIXON, P.M. Germination
and sporulation of Colletotrichum acutatum on symptomless
strawberry leaves. Phytopathology 91: 659–664,
2001
LEE, D.H.,
KIM, D.H., JEON, Y.A., UHM, J.Y., HONG, S.B. Molecular and
cultural characterization of Colletotrichum spp. causing
bitter rot of apples in Korea. Plant Pathology Journal 23: 37–44,
2007
LIM, T.K.; MANICOM, B.Q. Diseases of guava. In: PLOETZ, R.C. Diseases of
tropical fruit crops. Wallingford: University of Florida, 2003. p. 275-289
LIMA, K.S.C.; GROSSI, J.L.S.; LIMA, A.L.S.; ALVES, P.F.M.P.; CONEGLIAN,
R.C.C.; GODOY, R.L.O.; SABAA-SRUR, A.U.O. Efeito da irradiação ionizante γ na qualidade pós-colheita de
cenouras (Daucus carota L.) cv. Nantes.Ciência e Tecnologia de Alimentos,
v.21, p.202-208, 2001.
LOBUGLIO,
K.F., PFISTER, D.H. A Glomerella species
phylogenetically related to Colletotrichum acutatum on Norway
maple in Massachusetts. Mycologia 100: 710–715,
2008
LUBBE, C.M., DENMAN, S., CANNON, P.F., GROENEWALD, J.Z.,
LAMPRECHT, S.C., CROUS, P.W. Characterization of Colletotrichum species
associated with diseases of Proteaceae. Mycologia 96:
1268–1279, 2004
MADEIRA, M.C.B. Caracterização de
germoplasma de berinjela (Solanum melongena L.) e avaliação da resistência
a Colletotrichum gloesporioides (Penzig) Penzig et Saccardo. Dissertação (Mestrado)
- Universidade de Brasília, Brasil, DF, 1989. 267 p.
MANIRE, C.A., RHINEHART, H.L., SUTTON, D.A., THOMPSON,
E.H., RINALDI, M.G., BUCK, J.D., JACOBSON, E. Disseminated
mycotic infection caused by Colletotrichum
acutatum in a Kemp’s Ridley Sea Turtle (Lepidochelys kempi). Journal of
Clinical Microbiology 40: 4273–4280, 2002
MARCELINO, J., GIORDANO, R., GOULI, S., GOULI, V., PARKER,
B.L., SKINNER, M., TEBEEST, D., CESNIK, R. Colletotrichum acutatum var. fioriniae (teleomorph: Glomerella acutata var. fioriniae var. nov.)
infection of a scale insect. Mycologia 100: 353–374,
2008
MARTIN, F. W.; POLLACK, B. L. Eggplant,
Solanum melongena. New Orleans: USDA, 1979. 18 p. (USDA, Vegetables for the
hot, humid tropics, 5).
MCINNES,
T.B., BLACK, L.L., GATTI, J.M., JR. Disease-free plants for management
of strawberry anthracnose crown rot disease. Plant Disease 76: 260–264,
1992
MENDES, M.A.S., DA SILVA,
V.L., DIANESE, J.C., AND ET AL. Fungos
em Plantas no Brasil. Embrapa-SPI/Embrapa-Cenargen, Brasília, 555 pages, 1998
MORAES, S.R.G. Infecção e colonização de Colletotrichum gloeosporioides em goiana
e infecção de Colletotrichum acutatum em folhas de citros. Tese
(Doutorado em Fitopatologia) – Escola de Agricultura Luiz de Queiroz,
Universidade de São Paulo, Piracicaba. 114 p. 2009
NIRENBERG, H.I., FEILER, U.,
HAGEDORN G. Description of Colletotrichum lupini comb. nov. in
modern terms. Mycologia 94: 307–320, 2002
O'BEIRNE, D. Irradiation of fruits and vegetables: applications and
issues. Professional Horticulture, v.3, p.12-19, 1989.
PARIKKA,
P., PÄÄSKYNKIVI, E., LEMMETTY, A. Colletotrichum acutatum: survival in
plant debris and infection on alternate hosts. NJF Report 2(10): 37, 2006
PEREIRA, F.M.; MARTINEZ JÚNIOR, M. Goiabas
para industrialização. Jaboticabal:
Ed. Legis Summa, 142 p, 1986
PERES, N.A.,
MACKENZIE, S.J., PEEVER, T.L., TIMMER, L.W. Post bloom
fruit drop of citrus and Key lime anthracnose are caused by distinct
populations of Colletotrichum acutatum. Phytopathology 98: 345–352,
2008
PERES, N.A.,
TIMMER, L.W., ADASKAVEG, J.E., CORRELL, J.C. Life styles of Colletotrichum acutatum. Plant Disease 89: 784–796,
2005
PICCININ, E.; PASCHOLATI, S.F.; DI PIERO, R.M. Doenças da goiabeira. In:
KIMATI, H.; AMORIM, L.; REZENDE, J.A.M.; BERGAMIN, FILHO, A.; CAMARGO, L.E.A.
(Ed.). Manual de fitopatologia. 4 ed. São Paulo: Ceres, 2005. V. 2, cap.
44, p. 401-409
PONTE, J.J. Clínica de doenças de plantas.
Fortaleza: Edições UFC, 1996. 872 p.
PURSEGLOVE, J.W. Tropical crops: dicotyledon. London: Longman Group Limited,
719 p, 1968
RAHMAN, M.,
LOUWS, F.J. Colletotrichum
gloeosporioides on strawberry: From nursery to
fruiting field. In: Colletotrichum Diseases of Fruit
Crops (Peres NA, Timmer LW, editors. ,
eds). Pre-Congress workshop, ICPP, August 24, Torino, Italy: 54, 2008
REIFSCHNEIDER, F.J.B.; MADEIRA, M.C.B.;
RIBEIRO, S.C. Ciça: novo híbrido de berinjela resistente à antracnose e à
podridão-de-fomopsis. Horticultura Brasileira, Brasília, DF, v. 11, p. 57, 1993
RFLPs, and mating compatibility. Mycologia 95: 872–895, 2003
RIBEIRO, C.S.C.; BRUNE, S.;
REIFSCHNEIDER, F.J.B. Cultivo
da berinjela (Solanum melongena L.). Brasília, DF:
Embrapa Hortaliças, 1998. 23 p. (Embrapa Hortaliças. Instruções técnicas, 15).
SANCHEZ MARQUEZ, S., BILLS, G.F.,
ZABALGOGEAZCOA, I. The endophytic mycobiota of the grass Dactylis
glomerata. Fung. Diversity 27: 171-195, 2007
SANTOS, A. M. G.;
OLIVEIRA, S. M. A.; TERAO, D.; SILVA, J. M.; RODRIGUES, C. V. M. A.; SILVA, L.
L. Utilização de controle físico para o manejo pós-colheita da antracnose em
mangas. Tropical Plant Pathology 36 (Suplemento), agosto, XLIV Congresso
Brasileiro de Fitopatologia - Bento Gonçalves RS, 2011
SHIVAS,
R.G., TAN, Y.P. A taxonomic re-assessment of Colletotrichum acutatum, introducing C. fioriniae comb. et stat. nov. and C. simmondsii sp. nov. Fungal Diversity 39: 111–122,
2009
SILVA,
K.J.D. Distribuição e caracterização de isolados de Colletotrichum linde
muthianum no Brasil; Lavras: UFLA, 88 p: il, 2004
SIMMONDS, J.H. A study of the species of Colletotrichum causing ripe fruit rots in Queensland. Queensland
Journal of Agricultural and Animal Science 22: 437-459, 1965
SIMMONDS, J.H. Type specimens of Colletotrichum gloeosporioides var.
minor and Colletotrichum acutatum, Queensland Journal of
Agricultural and Animal Science 25: 178A, 1968
SREENIVASAPRASAD,
S., MILLS, P.R., BROWN, A.E. Nucleotide sequence of the rDNA
spacer 1 enables identification of isolates of Colletotrichum as C. acutatum. Mycological Research 98: 186–188,
1994
SREENIVASAPRASAD, S., MILLS, P.R., MEEHAN, B.M., BROWN,
A.E. Phylogeny and systematics of Colletotrichum species based on
ribosomal DNA spacer sequences. Genome 39: 499–512,
1996
SREENIVASAPRASAD, S., TALHINHAS, P. Genotypic and phenotypic diversity in Colletotrichum acutatum, a cosmopolitan pathogen causing anthracnose on a wide range
of hosts. Molecular
Plant Pathology 6: 361–378, 2005
TALGO, V.,
AAMOT, H.U., STROMENG, G.M., KLEMSDAL, S.S., STENSVAND, A. Glomerella acutata on highbush
blueberry (Vaccinium
corymbosum L.) in Norway. Online. Plant Health Progress doi:
10.1094/PHP-2007-0509-01-RS, 2007
TALHINHAS,
P., MOTA-CAPITÃO, C., MARTINS, S., RAMOS, A.P., NEVES-MARTINS, J.,
GUERRA-GUIMARÃES, L., VÁRZEA, V., SILVA, M.C., SREENIVASAPRASAD, S., OLIVEIRA,
H. Epidemiology, histopathology and a etiology of olive anthracnose caused
by Colletotrichum acutatum and C. gloeosporioides in Portugal. Plant Pathology 60:
483–495, 2011
TALHINHAS, P., SREENIVASAPRASAD, S., NEVES-MARTINS,
J., OLIVEIRA, H. Genetic and morphological
characterization of Colletotrichum
acutatum causing anthracnose of lupin. Phytopathology 92:
986–996, 2002
TALHINHAS, P., SREENIVASAPRASAD, S., NEVES-MARTINS, J.,
OLIVEIRA, H. Molecular and phenotypic analyses reveal
association of diverse Colletotrichum
acutatum groups and a low level of C. gloeosporioides with olive anthracnose. Applied and Environmental
Microbiology 71: 2987–2998, 2005
THAN, P. P., SHIVAS, R.G., JEEWON, R., PONGSUPASAMIT, S., MARNEY, T.S.,
TAYLOR, P.W.J., HYDE, K.D. Epitypification and phylogeny
of Colletotrichum acutatumJ.H. Simmonds. Fung. Diversity 28: 97-108, 2008
VAN DER AA,
H.A., NOORDELOOS, M.E., GRUYTER, J.D.E. Species concepts in some larger
genera of the coelomycetes. Studies in Mycology 32: 3–19, 1990.
VINNERE, O. Approches to species delineation in anamorphic (mitosporic)
fungi: A study on two extreme cases. Comprehensive Summaries of Uppsala
dissertations from the Faculty of Science and Technology, Uppsala, v. 917,
2004. 72 p. Disponível em:
acesso em 21 de junho de 2015.
WALLER, J. M. & SUTTON, B. C. Colletotrichum
acutatum. CMI Discriptions of
Patogenic Fungi and Bacteria, 630. In CAB International Mycologinal Institute,
Ferry Lane Kew, Surrey, UK, 1979.
WHARTON,
P.S., DIÉGUEZ-URIBEONDO, J. The biology of Colletotrichum acutatum. Anales del Jardín Botánico de Madrid 61: 3–22,
2004
WHARTON,
P.S., SCHILDER, A.M.C. Novel infection strategies of Colletotrichum acutatum on ripe
blueberry fruit. Plant Pathology 57: 122–134,
2008
XIA, H., WANG, X.-L., ZHU, H.-J., GAO, B.-D. First report of anthracnose
caused by Glomerella acutata on chili pepper in China. Pl. Dis. 95:
219, 2011
YANG, Y.L., LIU, Z.Y., CAI, L., HYDE, K.D., YU, Z.N., MCKENZIE,
E.H.C. Colletotrichum anthracnose of Amaryllidaceae. Fung. Diversity
39: 123-146, 2009





Nenhum comentário:
Postar um comentário
Observação: somente um membro deste blog pode postar um comentário.