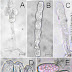
Hospedeiro: joá-de-capote, Nome científico do Hospedeiro: Nicandra physalodes, Família botânica: Solanaceae, Nome da doença: Cercosporiose, Agente causal: Cercospora nicandrae Chupp 1954, Local de coleta: Urutaí, GO, Data de coleta: 29/12/2024, Posicionamento Geográfico: 17o 29'8"S 48o12'47"O elevação 730 m.
Hospedeiro: joá-de-capote, Nome científico do Hospedeiro: Nicandra physalodes, Família botânica: Solanaceae, Nome da doença: Cercosporiose, Agente causal: Cercospora nicandrae Chupp 1954, Local de coleta: Urutaí, GO, Data de coleta: 29/12/2024, Posicionamento Geográfico: 17o 29'8"S 48o12'47"O elevação 730 m.
Hospedeiro: joá-de-capote, Nome científico do Hospedeiro: Nicandra physalodes, Família botânica: Solanaceae, Nome da doença: Cercosporiose, Agente causal: Cercospora nicandrae Chupp 1954, Local de coleta: Urutaí, GO, Data de coleta: 29/12/2024, Posicionamento Geográfico: 17o 29'8"S 48o12'47"O elevação 730 m.
Hospedeiro: joá-de-capote, Nome científico do Hospedeiro: Nicandra physalodes, Família botânica: Solanaceae, Nome da doença: Cercosporiose, Agente causal: Cercospora nicandrae Chupp 1954, Local de coleta: Urutaí, GO, Data de coleta: 29/12/2024, Posicionamento Geográfico: 17o 29'8"S 48o12'47"O elevação 730 m.
Crotalaria com desenvolvimento de fungo ectomicorrizico.

Hospedeiro: leiteiro, Nome científico do Hospedeiro: Euphorbia heterophylla, Família botânica: Euphorbiaceae, Nome da doença: helmintosporiose, Agente causal: Bipolaris euphorbiae (Hansf.) J.J. Muchovej & A.O. Carvalho, 1989, Local de coleta: Urutaí, GO, Data de coleta: 29/12/2024, Posicionamento Geográfico: 17o 29'8"S 48o12'47"O elevação 730 m.
Hospedeiro: leiteiro, Nome científico do Hospedeiro: Euphorbia heterophylla, Família botânica: Euphorbiaceae, Nome da doença: helmintosporiose, Agente causal: Bipolaris euphorbiae (Hansf.) J.J. Muchovej & A.O. Carvalho, 1989, Local de coleta: Urutaí, GO, Data de coleta: 29/12/2024, Posicionamento Geográfico: 17o 29'8"S 48o12'47"O elevação 730 m.
Hospedeiro: leiteiro, Nome científico do Hospedeiro: Euphorbia heterophylla, Família botânica: Euphorbiaceae, Nome da doença: helmintosporiose, Agente causal: Bipolaris euphorbiae (Hansf.) J.J. Muchovej & A.O. Carvalho, 1989, Local de coleta: Urutaí, GO, Data de coleta: 29/12/2024, Posicionamento Geográfico: 17o 29'8"S 48o12'47"O elevação 730 m.
Hospedeiro: leiteiro, Nome científico do Hospedeiro: Euphorbia heterophylla, Família botânica: Euphorbiaceae, Nome da doença: helmintosporiose, Agente causal: Bipolaris euphorbiae (Hansf.) J.J. Muchovej & A.O. Carvalho, 1989, Local de coleta: Urutaí, GO, Data de coleta: 29/12/2024, Posicionamento Geográfico: 17o 29'8"S 48o12'47"O elevação 730 m.
Hospedeiro: leiteiro, Nome científico do Hospedeiro: Euphorbia heterophylla, Família botânica: Euphorbiaceae, Nome da doença: helmintosporiose, Agente causal: Bipolaris euphorbiae (Hansf.) J.J. Muchovej & A.O. Carvalho, 1989, Local de coleta: Urutaí, GO, Data de coleta: 29/12/2024, Posicionamento Geográfico: 17o 29'8"S 48o12'47"O elevação 730 m.
Hospedeiro: leiteiro, Nome científico do Hospedeiro: Euphorbia heterophylla, Família botânica: Euphorbiaceae, Nome da doença: helmintosporiose, Agente causal: Bipolaris euphorbiae (Hansf.) J.J. Muchovej & A.O. Carvalho, 1989, Local de coleta: Urutaí, GO, Data de coleta: 29/12/2024, Posicionamento Geográfico: 17o 29'8"S 48o12'47"O elevação 730 m.
Hospedeiro: leiteiro, Nome científico do Hospedeiro: Euphorbia heterophylla, Família botânica: Euphorbiaceae, Nome da doença: helmintosporiose, Agente causal: Bipolaris euphorbiae (Hansf.) J.J. Muchovej & A.O. Carvalho, 1989, Local de coleta: Urutaí, GO, Data de coleta: 29/12/2024, Posicionamento Geográfico: 17o 29'8"S 48o12'47"O elevação 730 m.
Hospedeiro: leiteiro, Nome científico do Hospedeiro: Euphorbia heterophylla, Família botânica: Euphorbiaceae, Nome da doença: helmintosporiose, Agente causal: Bipolaris euphorbiae (Hansf.) J.J. Muchovej & A.O. Carvalho, 1989, Local de coleta: Urutaí, GO, Data de coleta: 29/12/2024, Posicionamento Geográfico: 17o 29'8"S 48o12'47"O elevação 730 m.
Hospedeiro: leiteiro, Nome científico do Hospedeiro: Euphorbia heterophylla, Família botânica: Euphorbiaceae, Nome da doença: helmintosporiose, Agente causal: Bipolaris euphorbiae (Hansf.) J.J. Muchovej & A.O. Carvalho, 1989, Local de coleta: Urutaí, GO, Data de coleta: 29/12/2024, Posicionamento Geográfico: 17o 29'8"S 48o12'47"O elevação 730 m.
Hospedeiro: figo, Nome científico do Hospedeiro: Ficus carica, Família botânica: Moraceae, Nome da doença: ferrugem, Agente causal: Cerotelium fici Castagne, (Arthur), 1917, Local de coleta: Urutaí, GO, Data de coleta: 29/12/2024, Posicionamento Geográfico: 17o 29'8"S 48o12'47"O elevação 730 m.
Hospedeiro: mandioca ou aipim, Nome científico do Hospedeiro: Ficus carica, Família botânica: Moraceae, Nome da doença: ferrugem, Agente causal: Xanthomonas phaseoli pv. manihotis (=Xanthomonas axonopodis pv manihotis (Bondar) Vauterin et al., 1995) ou X. cassavae, Local de coleta: Urutaí, GO, Data de coleta: 29/12/2024, Posicionamento Geográfico: 17o 29'8"S 48o12'47"O elevação 730 m.
Hospedeiro: mandioca ou aipim, Nome científico do Hospedeiro: Ficus carica, Família botânica: Moraceae, Nome da doença: ferrugem, Agente causal: Xanthomonas phaseoli pv. manihotis (=Xanthomonas axonopodis pv manihotis (Bondar) Vauterin et al., 1995) ou X. cassavae, Local de coleta: Urutaí, GO, Data de coleta: 29/12/2024, Posicionamento Geográfico: 17o 29'8"S 48o12'47"O elevação 730 m.
Hospedeiro: mandioca ou aipim, Nome científico do Hospedeiro: Ficus carica, Família botânica: Moraceae, Nome da doença: ferrugem, Agente causal: Xanthomonas phaseoli pv. manihotis (=Xanthomonas axonopodis pv manihotis (Bondar) Vauterin et al., 1995) ou X. cassavae, Local de coleta: Urutaí, GO, Data de coleta: 29/12/2024, Posicionamento Geográfico: 17o 29'8"S 48o12'47"O elevação 730 m.

Hospedeiro: mandioca ou aipim, Nome científico do Hospedeiro: Ficus carica, Família botânica: Moraceae, Nome da doença: ferrugem, Agente causal: Xanthomonas phaseoli pv. manihotis (=Xanthomonas axonopodis pv manihotis (Bondar) Vauterin et al., 1995) ou X. cassavae, Local de coleta: Urutaí, GO, Data de coleta: 29/12/2024, Posicionamento Geográfico: 17o 29'8"S 48o12'47"O elevação 730 m.
Hospedeiro: mandioca ou aipim, Nome científico do Hospedeiro: Ficus carica, Família botânica: Moraceae, Nome da doença: ferrugem, Agente causal: Xanthomonas phaseoli pv. manihotis (=Xanthomonas axonopodis pv manihotis (Bondar) Vauterin et al., 1995) ou X. cassavae, Local de coleta: Urutaí, GO, Data de coleta: 29/12/2024, Posicionamento Geográfico: 17o 29'8"S 48o12'47"O elevação 730 m.
Hospedeiro: capim colonião, Nome científico do Hospedeiro: Panicum maximum, Família botânica: Poaceae, Nome da doença: brusone, Agente causal: Pyricularia sp., Local de coleta: Urutaí, GO, Data de coleta: 29/12/2024, Posicionamento Geográfico: 17o 29'8"S 48o12'47"O elevação 730 m.
Hospedeiro: capim colchão, Nome científico do Hospedeiro: Digitaria horizontalis, Família botânica: Poaceae, Nome da doença: brusone, Agente causal: Pyricularia sp., Local de coleta: Urutaí, GO, Data de coleta: 29/12/2024, Posicionamento Geográfico: 17o 29'8"S 48o12'47"O elevação 730 m.
Hospedeiro: capim colchão, Nome científico do Hospedeiro: Digitaria horizontalis, Família botânica: Poaceae, Nome da doença: brusone, Agente causal: Pyricularia sp., Local de coleta: Urutaí, GO, Data de coleta: 29/12/2024, Posicionamento Geográfico: 17o 29'8"S 48o12'47"O elevação 730 m.
Hospedeiro: capim colchão, Nome científico do Hospedeiro: Digitaria horizontalis, Família botânica: Poaceae, Nome da doença: brusone, Agente causal: Pyricularia sp., Local de coleta: Urutaí, GO, Data de coleta: 29/12/2024, Posicionamento Geográfico: 17o 29'8"S 48o12'47"O elevação 730 m.
Hospedeiro: capim colchão, Nome científico do Hospedeiro: Digitaria horizontalis, Família botânica: Poaceae, Nome da doença: brusone, Agente causal: Pyricularia sp., Local de coleta: Urutaí, GO, Data de coleta: 29/12/2024, Posicionamento Geográfico: 17o 29'8"S 48o12'47"O elevação 730 m.